REKLAMA
Dziennik Ustaw - rok 2016 poz. 1960
ROZPORZĄDZENIE
MINISTRA SPRAWIEDLIWOŚCI
z dnia 21 listopada 2016 r.
w sprawie realizacji recept farmaceutycznych lub zapotrzebowań w aptekach szpitalnych i zakładowych podległych Ministrowi Sprawiedliwości oraz wydawania produktów leczniczych z tych aptek
Na podstawie art. 96 ust. 10 ustawy z dnia 6 września 2001 r. – Prawo farmaceutyczne (Dz. U. z 2008 r. poz. 271, z późn. zm.1)) zarządza się, co następuje:
§ 1. [Zakres regulacji]
1) sposób realizacji recept farmaceutycznych lub zapotrzebowań,
2) sposób sporządzania leku recepturowego lub aptecznego,
3) sposób wydawania z apteki produktów leczniczych, środków spożywczych specjalnego przeznaczenia żywieniowego lub wyrobów medycznych,
4) wzór zapotrzebowania na zakup produktów leczniczych, środków spożywczych specjalnego przeznaczenia żywieniowego lub wyrobów medycznych,
5) sposób i tryb ewidencjonowania recept farmaceutycznych i zapotrzebowań oraz wzór ewidencji recept farmaceutycznych i zapotrzebowań
– w aptekach szpitalnych i zakładowych podległych Ministrowi Sprawiedliwości.
§ 2. [Wydawanie produktów leczniczych, środków spożywczych lub wyrobów medycznych na podstawie zapotrzebowań zbiorczych lub imiennych]
2. Zapotrzebowania, o których mowa w ust. 1, są wystawiane w dwóch egzemplarzach.
§ 3. [Czynności wykonywane przed wydaniem produktu leczniczego, środka spożywczego specjalnego przeznaczenia żywieniowego lub wyrobu medycznego]
1) sprawdza prawidłowość wystawienia zapotrzebowania;
2) umieszcza na zapotrzebowaniu:
a) pieczęć apteki,
b) datę przyjęcia zapotrzebowania do realizacji,
c) datę realizacji zapotrzebowania,
d) swój podpis i swoją pieczątkę;
3) sprawdza termin ważności wydawanych produktów leczniczych, środków spożywczych specjalnego przeznaczenia żywieniowego lub wyrobów medycznych, o ile ich to dotyczy;
4) dokonuje kontroli wizualnej, jeżeli jest to możliwe, czy produkt leczniczy lub wyrób medyczny nie wykazują cech świadczących o ich niewłaściwej jakości, a w przypadku wyrobu medycznego – czy jest on zgodny z wymaganiami zasadniczymi, szczególnie w zakresie opakowania i oznakowania tych wyrobów;
5) udziela, w razie potrzeby, osobie odbierającej produkt leczniczy, środek spożywczy specjalnego przeznaczenia żywieniowego lub wyrób medyczny informacji co do sposobu ich stosowania i przechowywania oraz innych informacji dotyczących działania farmakologicznego i ewentualnych interakcji, w które mogą one wchodzić;
6) sprawdza, czy osoba, która zgłosiła się po odbiór produktów leczniczych, środków spożywczych specjalnego przeznaczenia żywieniowego lub wyrobów medycznych, została do tej czynności upoważniona;
7) żąda na zapotrzebowaniu podpisu i pieczątki osoby odbierającej z apteki produkty lecznicze, środki spożywcze specjalnego przeznaczenia żywieniowego lub wyroby medyczne;
8) odmawia wydania produktu leczniczego, środka spożywczego specjalnego przeznaczenia żywieniowego lub wyrobu medycznego, jeżeli:
a) zapotrzebowanie nie spełnia wymogów określonych w § 5,
b) zachodzi uzasadnione podejrzenie co do autentyczności zapotrzebowania,
c) jest konieczne dokonanie zmian, o których mowa w ust. 2, oraz zmian określonych w odrębnych przepisach, a nie ma możliwości porozumienia się z osobą, która wystawiła zapotrzebowanie.
2. Osoba realizująca zapotrzebowanie może:
1) wydać produkt w dawce mniejszej niż określona w zapotrzebowaniu, jeżeli dawka ta stanowi wielokrotność dawki, w której produkt jest wydawany, przy czym ilość substancji czynnej zawartej w produkcie wydawanym w dawce mniejszej ma łącznie odpowiadać ilości substancji czynnej zawartej w produkcie leczniczym lub wyrobie medycznym w dawce określonej w zapotrzebowaniu;
2) wydać produkt leczniczy, środek spożywczy specjalnego przeznaczenia żywieniowego lub wyrób medyczny będący odpowiednikiem odpowiednio produktu leczniczego, środka spożywczego specjalnego przeznaczenia żywieniowego lub wyrobu medycznego określonych w zapotrzebowaniu;
3) wydać produkt leczniczy w dawce najmniejszej dopuszczonej do obrotu na terytorium Rzeczypospolitej Polskiej, jeżeli na zapotrzebowaniu nie wpisano dawki produktu leczniczego.
3. Osoba realizująca zapotrzebowanie odnotowuje zmiany, o których mowa w ust. 2, przez umieszczenie na zapotrzebowaniu swojego podpisu i swojej pieczątki obok stosownej adnotacji oraz informuje o zmianach osobę, której produkt leczniczy, środek spożywczy specjalnego przeznaczenia żywieniowego lub wyrób medyczny są wydawane.
4. W przypadku nagłego zagrożenia zdrowia pacjenta farmaceuta posiadający prawo wykonywania zawodu może wystawić receptę farmaceutyczną i wydać bez zapotrzebowania produkt leczniczy zastrzeżony do wydawania na receptę, z wyłączeniem środków odurzających, substancji psychotropowych i prekursorów kategorii 1.
5. Do recepty farmaceutycznej stosuje się zasady określone w art. 96 ust. 4 pkt 1–3 i 5 ustawy z dnia 6 września 2001 r. – Prawo farmaceutyczne.
§ 4. [Lek recepturowy]
1) stosuje, z zastrzeżeniem pkt 2, surowce farmaceutyczne niezbędne do przygotowania danej postaci leku recepturowego;
2) stosuje surowiec o najniższym stężeniu, jeżeli na zapotrzebowaniu – jako wchodzący w skład leku recepturowego – został wymieniony surowiec farmaceutyczny występujący w kilku stężeniach, a stężenie tego surowca nie zostało określone;
3) dokonuje korekty składu leku recepturowego, jeżeli podany w zapotrzebowaniu skład może tworzyć niezgodność chemiczną lub fizyczną, mogącą zmienić działanie leku lub jego wygląd, przez:
a) dodanie surowca farmaceutycznego ułatwiającego prawidłowe przygotowanie postaci leku recepturowego lub pozwalającego na uzyskanie jednolitego dawkowania,
b) prawidłowy dobór surowców farmaceutycznych zapewniający rozpuszczenie wszystkich składników leku recepturowego w celu uzyskania właściwej postaci,
c) zmianę postaci surowca farmaceutycznego z rozpuszczalnej na nierozpuszczalną lub odwrotnie, z uwzględnieniem koniecznej różnicy w ilości surowca;
4) zmniejsza ilość surowca farmaceutycznego w składzie leku recepturowego do ilości określonej przez dawkę maksymalną, jeżeli:
a) dawka maksymalna jest dla tego surowca ustalona,
b) ze składu oraz sposobu użycia podanego w zapotrzebowaniu wynika, że nastąpiło przekroczenie dawki maksymalnej, a wystawiający zapotrzebowanie nie dokonał adnotacji o konieczności zastosowania dawki wskazanej w składzie leku;
5) dokonuje na recepcie farmaceutycznej lub zapotrzebowaniu adnotacji o dacie i godzinie sporządzenia leku recepturowego oraz umieszcza swój podpis i swoją pieczątkę.
2. Surowce farmaceutyczne i postać leku recepturowego, o których mowa w ust. 1 pkt 1, muszą spełniać wymagania określone w Farmakopei Polskiej lub Farmakopei Europejskiej, lub innych odpowiednich farmakopeach uznawanych w państwach członkowskich Unii Europejskiej.
3. Osoba sporządzająca lek recepturowy może dokonać zmian innych niż wymienione w ust. 1 pkt 3 i 4 jedynie po porozumieniu się z osobą, która wystawiła zapotrzebowanie.
4. Osoba sporządzająca lek recepturowy odnotowuje na zapotrzebowaniu dokonane zmiany oraz umieszcza na nich swój podpis i swoją pieczątkę.
5. Przepisy ust. 1, 2 i 4 stosuje się odpowiednio w przypadku osoby sporządzającej lek apteczny.
§ 5. [Wzór zapotrzebowania zbiorczego i imiennego]
2. Wzór zapotrzebowania imiennego na produkty lecznicze, środki spożywcze specjalnego przeznaczenia żywieniowego lub wyroby medyczne jest określony w załączniku nr 2 do rozporządzenia.
§ 6. [Ewidencja recept farmaceutycznych]
2. Ewidencja recept farmaceutycznych i zapotrzebowań jest prowadzona w formie elektronicznej, zabezpieczonej przed dostępem osób nieuprawnionych, według dat ich sporządzenia. Ewidencję przechowuje się przez okres 5 lat, licząc od końca roku kalendarzowego, w którym została sporządzona. Dopuszcza się prowadzenie ewidencji w formie papierowej.
§ 7. [Wzór ewidencji recept farmaceutycznych i zapotrzebowań]
2. Wzór ewidencji zapotrzebowań jest określony w załączniku nr 4 do rozporządzenia.
§ 8. [Wejście w życie]
Minister Sprawiedliwości: Z. Ziobro
1) Zmiany tekstu jednolitego wymienionej ustawy zostały ogłoszone w Dz. U. z 2008 r. poz. 1505 i 1570, z 2009 r. poz. 97, 206, 753, 788 i 817, z 2010 r. poz. 513 i 679, z 2011 r. poz. 322, 451, 622, 654, 657 i 696, z 2012 r. poz. 1342 i 1544, z 2013 r. poz. 1245, z 2014 r. poz. 822 i 1491, z 2015 r. poz. 28, 277, 788, 875, 1771, 1830, 1918, 1926 i 1991 oraz z 2016 r. poz. 823, 960, 1579 i 1948.
2) Niniejsze rozporządzenie było poprzedzone rozporządzeniem Ministra Sprawiedliwości z dnia 26 lutego 2003 r. w sprawie wydawania produktów leczniczych i wyrobów medycznych z aptek zakładowych w zakładach opieki zdrowotnej dla osób pozbawionych wolności (Dz. U. poz. 608), które traci moc z dniem wejścia w życie niniejszego rozporządzenia na podstawie art. 48 ust. 1 pkt 7 ustawy z dnia 9 października 2015 r. o zmianie ustawy o systemie informacji w ochronie zdrowia oraz niektórych innych ustaw (Dz. U. poz. 1991 oraz z 2016 r. poz. 65, 580, 652, 832 i 1579).
Załączniki do rozporządzenia Ministra Sprawiedliwości
z dnia 21 listopada 2016 r. (poz. 1960)
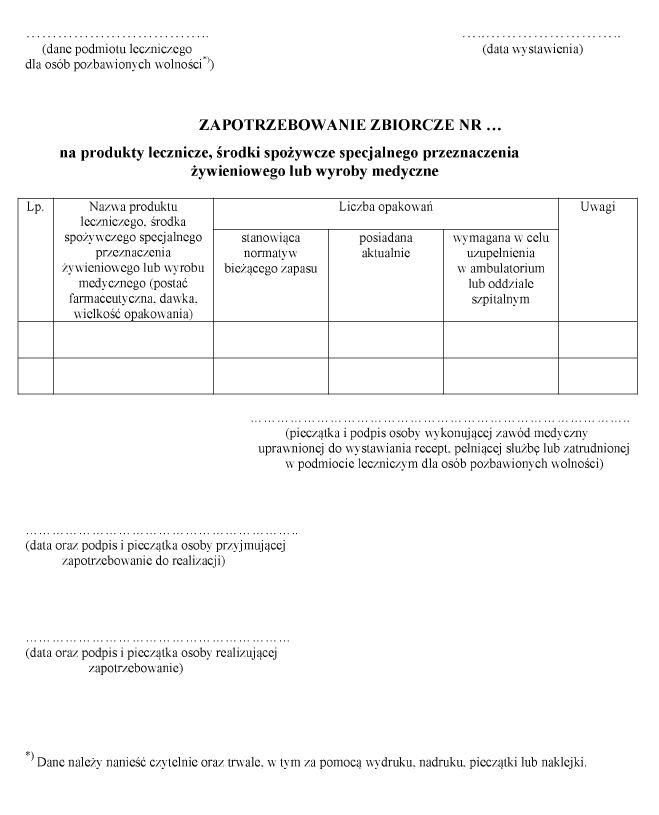
Załącznik nr 1
WZÓR – ZAPOTRZEBOWANIE ZBIORCZE NA PRODUKTY LECZNICZE, ŚRODKI SPOŻYWCZE SPECJALNEGO PRZEZNACZENIA ŻYWIENIOWEGO LUB WYROBY MEDYCZNE
Załącznik nr 2
WZÓR – ZAPOTRZEBOWANIE IMIENNE NA PRODUKTY LECZNICZE, ŚRODKI SPOŻYWCZE SPECJALNEGO PRZEZNACZENIA ŻYWIENIOWEGO LUB WYROBY MEDYCZNE

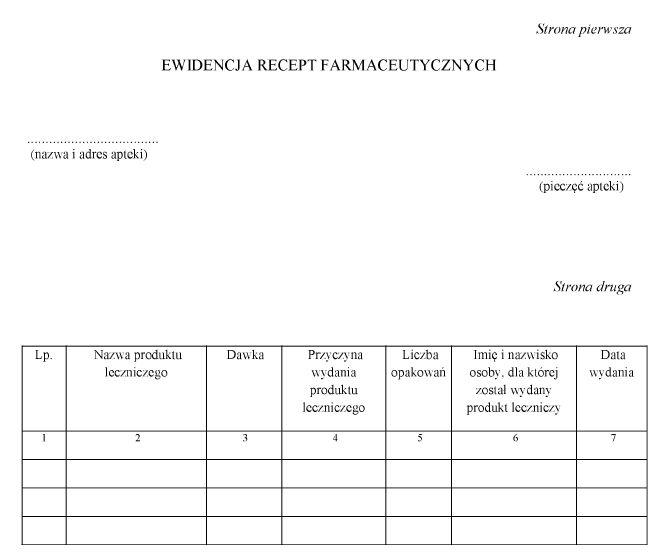
Załącznik nr 3
WZÓR – EWIDENCJA RECEPT FARMACEUTYCZNYCH
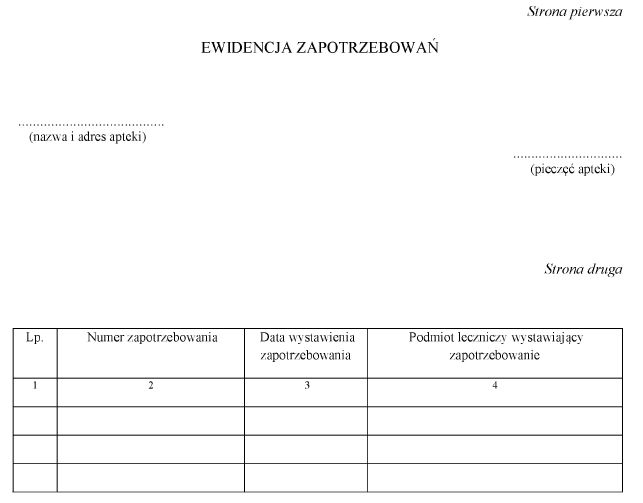
Załącznik nr 4
WZÓR – EWIDENCJA ZAPOTRZEBOWAŃ
- Data ogłoszenia: 2016-12-05
- Data wejścia w życie: 2016-12-20
- Data obowiązywania: 2016-12-20
- Dokument traci ważność: 2018-04-18
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA
