REKLAMA
Dziennik Ustaw - rok 2021 poz. 1885
OBWIESZCZENIE
MINISTRA ZDROWIA
z dnia 27 września 2021 r.
w sprawie ogłoszenia jednolitego tekstu rozporządzenia Ministra Zdrowia w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii
1. Na podstawie art. 16 ust. 3 ustawy z dnia 20 lipca 2000 r. o ogłaszaniu aktów normatywnych i niektórych innych aktów prawnych (Dz. U. z 2019 r. poz. 1461) ogłasza się w załączniku do niniejszego obwieszczenia jednolity tekst rozporządzenia Ministra Zdrowia z dnia 23 marca 2011 r. w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii (Dz. U. poz. 437), z uwzględnieniem zmian wprowadzonych rozporządzeniem Ministra Zdrowia z dnia 21 grudnia 2019 r. zmieniającym rozporządzenie w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii (Dz. U. poz. 2499).
2. Podany w załączniku do niniejszego obwieszczenia tekst jednolity rozporządzenia nie obejmuje § 2 i § 3 rozporządzenia Ministra Zdrowia z dnia 21 grudnia 2019 r. zmieniającego rozporządzenie w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii (Dz. U. poz. 2499), które stanowią:
"§ 2. 1. Rejestr produktów objętych powiadomieniem, wpisanych do rejestru przed dniem wejścia w życie niniejszego rozporządzenia, prowadzi się według wzoru określonego w rozporządzeniu zmienianym w § 1 w brzmieniu dotychczasowym.
2. Wpisy w rejestrze produktów objętych powiadomieniem, dokonane przed dniem wejścia w życie niniejszego rozporządzenia, w przypadku których w kolumnie nr 9 użyto sformułowania "PWT - postępowanie w toku", dostosowuje się do wymogów niniejszego rozporządzenia w terminie do dnia 31 grudnia 2022 r.
§ 3. Rozporządzenie wchodzi w życie z dniem 1 stycznia 2020 r.".
Minister Zdrowia: wz. W. Kraska
Załącznik do obwieszczenia Ministra Zdrowia
z dnia 27 września 2021 r. (poz. 1885)
ROZPORZĄDZENIE
MINISTRA ZDROWIA1)
z dnia 23 marca 2011 r.
w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii2) I), 2a) II)
Na podstawie art. 31 ust. 6 ustawy z dnia 25 sierpnia 2006 r. o bezpieczeństwie żywności i żywienia (Dz. U. z 2020 r. poz. 2021) zarządza się, co następuje:
§ 1. Rozporządzenie określa:
1) wzór formularza powiadomienia, o którym mowa w art. 29 ust. 4 ustawy z dnia 25 sierpnia 2006 r. o bezpieczeństwie żywności i żywienia, zwanej dalej "ustawą";
2) dane zawarte w rejestrze produktów objętych powiadomieniem umożliwiające ich identyfikację;
3) wzór rejestru, o którym mowa w pkt 2;
4) wykaz krajowych jednostek naukowych właściwych do wydawania opinii, o której mowa w art. 31 ust. 1 pkt 2 ustawy, zwanej dalej "opinią";
5) metody obliczania kosztów ponoszonych przez krajową jednostkę naukową w związku z wydaniem opinii;
6) wysokość opłaty pobieranej przy wydawaniu opinii przez Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych.
§ 2. 1. Wzór elektronicznego formularza powiadomienia Głównego Inspektora Sanitarnego przez podmiot działający na rynku spożywczym o pierwszym wprowadzeniu lub o zamiarze wprowadzenia do obrotu na terytorium Rzeczypospolitej Polskiej produktu jako środka spożywczego, zwanego dalej "powiadomieniem", został określony w załączniku nr 1 do rozporządzenia.
2.3) Elektroniczny formularz powiadomienia, o którym mowa w ust. 1, znajduje się na stronie internetowej Głównego Inspektoratu Sanitarnego.
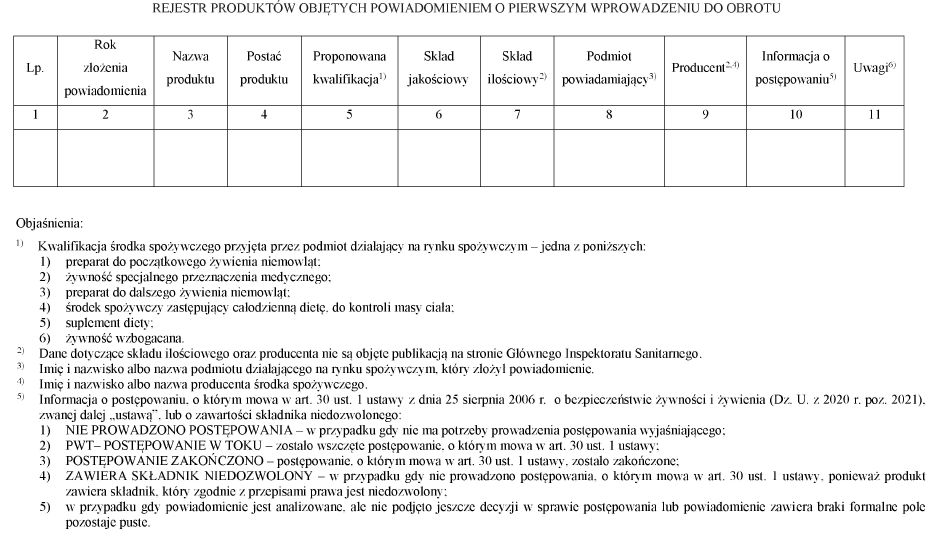
§ 3. 1.4) Rejestr produktów objętych powiadomieniem zawiera następujące dane:
1) rok złożenia powiadomienia;
2) nazwę produktu;
3) postać produktu, w jakiej jest on wprowadzany do obrotu;
4) kwalifikację zaproponowaną przez podmiot działający na rynku spożywczym;
5) skład jakościowy obejmujący dane dotyczące składników zawartych w produkcie, w tym substancji czynnych;
6) skład ilościowy składników;
7) imię i nazwisko albo nazwę podmiotu powiadamiającego o pierwszym wprowadzeniu do obrotu;
8) imię i nazwisko albo nazwę producenta;
9) informację o postępowaniu, o którym mowa w art. 30 ust. 1 ustawy, lub o zawartości składnika niedozwolonego;
10) uwagi - informacje dodatkowe o danym przypadku, w sytuacji gdy postępowanie, o którym mowa w art. 30 ust. 1 ustawy, nie było prowadzone, zostało zakończone lub produkt zawiera składnik niedozwolony.
2. Dane z rejestru, o którym mowa w ust. 1, są publikowane na stronie internetowej Głównego Inspektoratu Sanitarnego, z wyłączeniem danych stanowiących tajemnicę przedsiębiorcy.
§ 4. Wzór rejestru produktów, o którym mowa w § 3, został określony w załączniku nr 2 do rozporządzenia.
§ 5. Wykaz krajowych jednostek naukowych właściwych do wydania opinii został określony w załączniku nr 3 do rozporządzenia.
§ 6. Koszty ponoszone przez krajową jednostkę naukową wydającą opinię obejmują koszty osobowe i rzeczowe.
§ 7. Koszty osobowe obejmują koszty wynagrodzeń pracowników opracowujących opinie, w tym koszty ponoszone przez pracodawcę, zgodnie z obowiązującymi przepisami dotyczącymi wypłaty wynagrodzeń, podatki i inne opłaty stanowiące należności od tych wynagrodzeń.
§ 8. Przyjmuje się, że czas niezbędny do przygotowania opinii o jednym produkcie wynosi średnio 15-17 godzin pracy pracowników.
§ 9. Koszty rzeczowe obejmują koszty administracyjno-biurowe utrzymania krajowej jednostki naukowej obliczane proporcjonalnie do nakładu czasu pracy niezbędnego do przygotowania opinii.
§ 10. 1. Wysokość opłaty pobieranej przy wydawaniu opinii przez Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych wynosi 2700 złotych.
2. Opłata, o której mowa w ust. 1, dotyczy jednego produktu.
§ 11. Rozporządzenie wchodzi w życie po upływie 14 dni od dnia ogłoszenia5).6)
Załączniki do rozporządzenia Ministra Zdrowia
z dnia 23 marca 2011 r.
Załącznik nr 17)
WZÓR - POWIADOMIENIE O WPROWADZENIU/O ZAMIARZE WPROWADZENIA PO RAZ PIERWSZY DO OBROTU NA TERYTORIUM RZECZYPOSPOLITEJ POLSKIEJ


Załącznik nr 27)
WZÓR - REJESTR PRODUKTÓW OBJĘTYCH POWIADOMIENIEM O PIERWSZYM WPROWADZENIU DO OBROTU

Załącznik nr 3
WYKAZ KRAJOWYCH JEDNOSTEK NAUKOWYCH WŁAŚCIWYCH DO WYDAWANIA OPINII
| Nazwa krajowej jednostki naukowej | Adres |
| Instytut Matki i Dziecka | ul. Kasprzaka 17a, 01-211 Warszawa |
| Instytut Żywności i Żywienia im. prof. dr med. Aleksandra Szczygła | ul. Powsińska 61/63, 02-903 Warszawa |
| Narodowy Instytut Zdrowia Publicznego - Państwowy Zakład Higieny | ul. Chocimska 24, 00-791 Warszawa |
| Instytut "Pomnik - Centrum Zdrowia Dziecka" | al. Dzieci Polskich 20, 04-730 Warszawa-Międzylesie |
| Instytut Włókien Naturalnych i Roślin Zielarskich | ul. Wojska Polskiego 71B, 60-630 Poznań |
| Narodowy Instytut Leków | ul. Chełmska 30/34, 00-725 Warszawa |
| Państwowy Instytut Weterynaryjny - Państwowy Instytut Badawczy | ul. Al. Partyzantów 57, 24-100 Puławy |
| Instytut Medycyny Wsi im. Witolda Chodźki | ul. Jaczewskiego 2, 20-950 Lublin |
| Instytut Sportu | ul. Trylogii 2/16, 01-982 Warszawa |
1) Minister Zdrowia kieruje działem administracji rządowej - zdrowie, na podstawie § 1 ust. 2 rozporządzenia Prezesa Rady Ministrów z dnia 27 sierpnia 2020 r. w sprawie szczegółowego zakresu działania Ministra Zdrowia (Dz. U. z 2021 r. poz. 932).
I) Pkt 3 uchylony przez § 1 pkt 1 rozporządzenia Ministra Zdrowia z dnia 21 grudnia 2019 r. zmieniającego rozporządzenie w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii (Dz. U. poz. 2499), które weszło w życie z dniem 1 stycznia 2020 r.
2) Rozporządzenie wdraża częściowo w zakresie swojej właściwości następujące dyrektywy:
1) dyrektywę Komisji 1999/21/WE z dnia 25 marca 1999 r. w sprawie dietetycznych środków spożywczych specjalnego przeznaczenia medycznego (Dz. Urz. WE L 91 z 07.04.1999, str. 29; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 13, t. 23, str. 273);
2) dyrektywę 2002/46/WE Parlamentu Europejskiego i Rady z dnia 10 czerwca 2002 r. w sprawie zbliżenia ustawodawstw Państw Członkowskich odnoszących się do suplementów żywnościowych (Dz. Urz. WE L 183 z 12.07.2002, str. 51, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 13, t. 29, str. 490);
3) (uchylony);
4) dyrektywę Komisji 2006/141/WE z dnia 22 grudnia 2006 r. w sprawie preparatów do początkowego żywienia niemowląt i preparatów do dalszego żywienia niemowląt oraz zmieniającą dyrektywę 1999/21/WE (Dz. Urz. WE L 401 z 30.12.2006, str. 1).
II) Dodany przez § 1 pkt 2 rozporządzenia, o którym mowa w odnośniku I.
2a) Niniejsze rozporządzenie służy stosowaniu:
1) rozporządzenia Parlamentu Europejskiego i Rady (UE) nr 609/2013 z dnia 12 czerwca 2013 r. w sprawie żywności przeznaczonej dla niemowląt i małych dzieci oraz żywności specjalnego przeznaczenia medycznego i środków spożywczych zastępujących całodzienną dietę, do kontroli masy ciała oraz uchylającego dyrektywę Rady 92/52/EWG, dyrektywy Komisji 96/8/WE, 1999/21/WE, 2006/125/WE i 2006/141/WE, dyrektywę Parlamentu Europejskiego i Rady 2009/39/WE oraz rozporządzenia Komisji (WE) nr 41/2009 i (WE) nr 953/2009 (Dz. Urz. UE L 181 z 29.06.2013, str. 35, Dz. Urz. UE L 349 z 05.12.2014, str. 67 oraz Dz. Urz. UE L 158 z 21.06.2017, str. 5);
2) rozporządzenia delegowanego Komisji (UE) 2016/127 z dnia 25 września 2015 r. uzupełniającego rozporządzenie Parlamentu Europejskiego i Rady (UE) nr 609/2013 w odniesieniu do szczegółowych wymogów dotyczących składu preparatów do początkowego żywienia niemowląt i preparatów do dalszego żywienia niemowląt oraz informacji na ich temat, a także w odniesieniu do informacji dotyczących żywienia niemowląt i małych dzieci (Dz. Urz. UE L 25 z 02.02.2016, str. 1, Dz. Urz. UE L 94 z 12.04.2018, str. 1 oraz Dz. Urz. UE L 137 z 23.05.2019, str. 12);
3) rozporządzenia delegowanego Komisji (UE) 2016/128 z dnia 25 września 2015 r. uzupełniającego rozporządzenie Parlamentu Europejskiego i Rady (UE) nr 609/2013 w odniesieniu do szczegółowych wymogów dotyczących składu żywności specjalnego przeznaczenia medycznego oraz informacji na jej temat (Dz. Urz. UE L 25 z 02.02.2016, str. 30);
4) rozporządzenia delegowanego Komisji (UE) 2017/1798 z dnia 2 czerwca 2017 r. uzupełniającego rozporządzenie Parlamentu Europejskiego i Rady (UE) nr 609/2013 w odniesieniu do szczegółowych wymogów dotyczących składu i informacji w odniesieniu do środków spożywczych zastępujących całodzienną dietę, do kontroli masy ciała (Dz. Urz. UE L 259 z 07.10.2017, str. 2).
3) Ze zmianą wprowadzoną przez § 1 pkt 3 rozporządzenia Ministra Zdrowia z dnia 21 grudnia 2019 r. zmieniającego rozporządzenie w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii (Dz. U. poz. 2499), które weszło w życie z dniem 1 stycznia 2020 r.
4) W brzmieniu ustalonym przez § 1 pkt 4 rozporządzenia, o którym mowa w odnośniku 3.
5) Rozporządzenie zostało ogłoszone w dniu 15 kwietnia 2011 r.
6) Niniejsze rozporządzenie było poprzedzone rozporządzeniem Ministra Zdrowia z dnia 20 czerwca 2007 r. w sprawie rejestru produktów wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej jako środki spożywcze, wzoru powiadomienia oraz metod obliczania kosztów związanych z wydaniem opinii o tych produktach (Dz. U. poz. 830), które utraciło moc z dniem wejścia w życie niniejszego rozporządzenia na podstawie art. 9 ustawy z dnia 8 stycznia 2010 r. o zmianie ustawy o bezpieczeństwie żywności i żywienia oraz niektórych innych ustaw (Dz. U. poz. 105).
7) W brzmieniu ustalonym przez § 1 pkt 5 rozporządzenia, o którym mowa w odnośniku 3.
- Data ogłoszenia: 2021-10-18
- Data wejścia w życie: 2021-10-18
- Data obowiązywania: 2021-10-18
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA
