REKLAMA
Dziennik Ustaw - rok 2016 poz. 208
ROZPORZĄDZENIE
MINISTRA ZDROWIA1)
z dnia 17 lutego 2016 r.
w sprawie wzorów wniosków związanych z badaniem klinicznym wyrobu medycznego lub aktywnego wyrobu medycznego do implantacji oraz wysokości opłat za złożenie tych wniosków
Na podstawie art. 50 ustawy z dnia 20 maja 2010 r. o wyrobach medycznych (Dz. U. z 2015 r. poz. 876 i 1918) zarządza się, co następuje:
§ 1. [Zakres regulacji]
1) wzór wniosku o wydanie pozwolenia na prowadzenie badania klinicznego i o wydanie opinii przez komisję bioetyczną o badaniu klinicznym;
2) wzór wniosku o wydanie pozwolenia na wprowadzenie zmian w badaniu klinicznym i o wydanie opinii przez komisję bioetyczną o wnioskowanych zmianach w badaniu klinicznym;
3) wysokość opłaty za złożenie wniosku o wydanie pozwolenia na prowadzenie badania klinicznego;
4) wysokość opłaty za złożenie wniosku o wydanie pozwolenia na wprowadzenie zmian w badaniu klinicznym.
§ 2. [Wzór wniosku o wydanie pozwolenia]
2. Wzór wniosku o wydanie pozwolenia na wprowadzenie zmian w badaniu klinicznym i o wydanie opinii przez komisję bioetyczną o wnioskowanych zmianach w badaniu klinicznym jest określony w załączniku nr 2 do rozporządzenia.
§ 3. [Opłaty za złożenie wniosku]
1) na prowadzenie badania klinicznego – 5000 złotych;
2) na wprowadzenie zmian w badaniu klinicznym – 1500 złotych.
§ 4. [Wejście w życie]
Minister Zdrowia: K. Radziwiłł
1) Minister Zdrowia kieruje działem administracji rządowej - zdrowie, na podstawie § 1 ust. 2 rozporządzenia Prezesa Rady Ministrów z dnia 17 listopada 2015 r. w sprawie szczegółowego zakresu działania Ministra Zdrowia (Dz. U. poz. 1908).
2) Niniejsze rozporządzenie było poprzedzone rozporządzeniem Ministra Zdrowia z dnia 15 listopada 2010 r. w sprawie wzorów wniosków przedkładanych w związku z badaniem klinicznym, wysokości opłat za złożenie wniosków oraz sprawozdania końcowego z wykonania badania klinicznego (Dz. U. Nr 222, poz. 1453), które traci moc z dniem 20 lutego 2016 r. w związku z wejściem w życie ustawy z dnia 11 września 2015 r. o zmianie ustawy o wyrobach medycznych oraz niektórych innych ustaw (Dz. U. poz. 1918).
Załączniki do rozporządzenia Ministra Zdrowia
z dnia 17 lutego 2016 r. (poz. 208)
Załącznik nr 1
WZÓR – WNIOSEK O WYDANIE POZWOLENIA NA PROWADZENIE BADANIA KLINICZNEGO / WNIOSEK O WYDANIE OPINII PRZEZ KOMISJĘ BIOETYCZNĄ O BADANIU KLINICZNYM





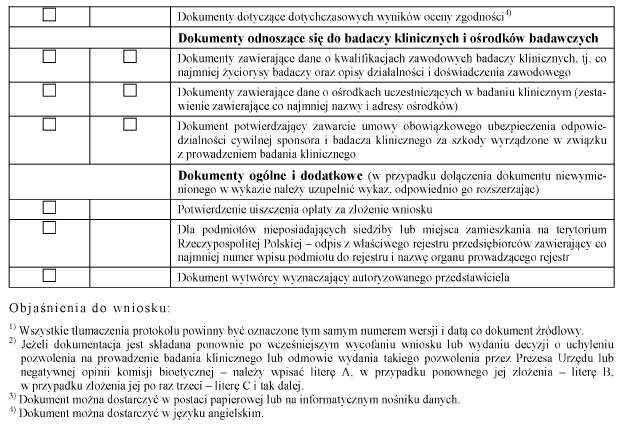
Załącznik nr 2
WZÓR – WNIOSEK O WYDANIE POZWOLENIA NA WPROWADZENIE ZMIAN W BADANIU KLINICZNYM / WNIOSEK O WYDANIE OPINII PRZEZ KOMISJĘ BIOETYCZNĄ O WNIOSKOWANYCH ZMIANACH W BADANIU KLINICZNYM




- Data ogłoszenia: 2016-02-19
- Data wejścia w życie: 2016-02-20
- Data obowiązywania: 2016-02-20
- Dokument traci ważność: 2022-05-26
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA
