REKLAMA
Dziennik Ustaw - rok 2011 nr 82 poz. 452
ROZPORZĄDZENIE RADY MINISTRÓW
z dnia 23 marca 2011 r.
w sprawie wprowadzenia na 2011 r. programów zwalczania wścieklizny i gąbczastej encefalopatii bydła oraz programu mającego na celu wykrycie występowania zakażeń wirusami wywołującymi grypę ptaków oraz poszerzenie wiedzy na temat ryzyka wystąpienia tej choroby
Na podstawie art. 57 ust. 7 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (Dz. U. z 2008 r. Nr 213, poz. 1342 oraz z 2010 r. Nr 47, poz. 278, Nr 60, poz. 372 i Nr 78, poz. 513) zarządza się, co następuje:
1) zwalczania:
a) wścieklizny (Rabies), który jest określony w załączniku nr 1 do rozporządzenia,
b) gąbczastej encefalopatii bydła (Bovine spongiform encephalopathy – BSE), który jest określony w załączniku nr 2 do rozporządzenia;
2) mający na celu wykrycie występowania zakażeń wirusami wywołującymi grypę ptaków (Avian influenza) oraz poszerzenie wiedzy na temat ryzyka wystąpienia tej choroby, który jest określony w załączniku nr 3 do rozporządzenia.
Prezes Rady Ministrów: D. Tusk
Załączniki do rozporządzenia Rady Ministrów
z dnia 23 marca 2011 r. (poz. 452)
Załącznik nr 1
PROGRAM ZWALCZANIA WŚCIEKLIZNY (RABIES)
1. Identyfikacja programu
Państwo członkowskie: Rzeczpospolita Polska
Choroba: wścieklizna (Rabies)
Wniosek o współfinansowanie na rok: 2011
Wysłano do Komisji Europejskiej dnia: 30 kwietnia 2010 r.
2. Dane historyczne dotyczące sytuacji epizootycznej w zakresie wścieklizny
W okresie międzywojennym oraz w pierwszych latach po II wojnie światowej głównym nosicielem wścieklizny na terytorium Rzeczypospolitej Polskiej były psy. Wprowadzenie w 1949 r. obowiązkowego szczepienia psów przeciwko wściekliźnie pozwoliło na opanowanie problemu występowania tej choroby. Liczba przypadków wścieklizny wśród zwierząt obniżyła się z ponad 3600 w 1946 r. do 73 przypadków w 1956 r. Problem wścieklizny ponownie się pojawił, kiedy zaczęto rejestrować coraz więcej przypadków tej choroby w środowisku zwierząt wolno żyjących. W latach 1946–1956 zgłaszano rocznie od 1 do 6 przypadków wścieklizny wśród zwierząt dzikich. W 1956 r. i 1957 r. nie zanotowano żadnego przypadku wścieklizny u zwierząt dzikich. W latach następnych zauważalny był wzrost zachorowań wśród zwierząt dzikich, a w szczególności u lisów. Pod koniec lat siedemdziesiątych zachorowania u zwierząt dzikich przekraczały liczbę zachorowań u zwierząt domowych.
W 1990 r. w Rzeczypospolitej Polskiej stwierdzono 2045 przypadków wścieklizny, w tym 1668 przypadków wśród zwierząt dzikich (1374 przypadki u lisów). Najwięcej przypadków wścieklizny zanotowano w ówczesnych województwach: poznańskim (157), opolskim (139), koszalińskim (133), szczecińskim (130), bydgoskim (123), słupskim (103). Nie notowano ich w bialskopodlaskim, a pojedyncze przypadki odnotowano w lubelskim, łomżyńskim, łódzkim, przemyskim.
W 1991 r. stwierdzono 2287 przypadków wścieklizny, w tym 1864 u zwierząt dzikich, z czego 1513 przypadków u lisów. Wścieklizny nie odnotowano w ówczesnym województwie lubelskim, a pojedyncze przypadki wystąpiły w przemyskim, łódzkim, łomżyńskim, krośnieńskim.
W 1992 r. stwierdzono 3084 przypadki wścieklizny, w tym u zwierząt dzikich 2549, z czego 2079 u lisów.
Z uwagi na rozprzestrzenianie się wścieklizny w 1993 r. rozpoczęto akcję doustnych szczepień lisów wolno żyjących przeciwko wściekliźnie.
W 1993 r. stwierdzono 2648 przypadków wścieklizny u zwierząt, w tym 2166 u zwierząt dzikich, z czego 1803 u lisów.
W 1994 r. stwierdzono 2238 przypadków wścieklizny u zwierząt, w tym u zwierząt dzikich 1788, z czego 1506 u lisów.
W 1995 r. stwierdzono 1973 przypadki u zwierząt, w tym 1528 u zwierząt dzikich, z czego 1280 u lisów.
W 1996 r. stwierdzono 2527 przypadków u zwierząt, w tym 2064 u zwierząt dzikich, z czego 1779 u lisów.
W 1997 r. stwierdzono 1494 przypadki u zwierząt, w tym 1239 u zwierząt dzikich, z czego 1091 u lisów.
Efektem nieustającego przeprowadzania szczepień w zachodniej części terytorium Rzeczypospolitej Polskiej był spadek liczby przypadków wścieklizny, a zwłaszcza bardziej zadowalający fakt braku jej występowania od dłuższego czasu na obszarach województw: zachodniopomorskiego, lubuskiego i dolnośląskiego.
W 1998 r. stwierdzono 1329 przypadków u zwierząt, w tym 1120 u zwierząt dzikich, z czego 927 u lisów.
W 1999 r. stwierdzono 1148 przypadków u zwierząt, w tym 721 u lisów.
W 2000 r. stwierdzono 2224 przypadki u zwierząt, w tym u lisów 1583, a w 2001 r. stwierdzono 2964 przypadki u zwierząt, w tym u lisów 2224.
W trakcie przeprowadzanych akcji szczepień zaobserwowano „przemieszczanie się” wścieklizny do wschodniej części terytorium Rzeczypospolitej Polskiej, czyli na obszary nieobjęte do tej pory szczepieniami, oraz występowanie pojedynczych przypadków wścieklizny na terenach przygranicznych z Republiką Czeską.
W 2002 r. liczba przypadków wścieklizny u zwierząt na terytorium Rzeczypospolitej Polskiej wyniosła 1119, z czego 1038 przypadków zanotowano u zwierząt dzikich, w tym 884 u lisów. W 2002 r. największą liczbę przypadków wścieklizny zanotowano w województwie wielkopolskim – 339 przypadków.
W 2003 r. stwierdzono 388 przypadków u zwierząt, w tym 314 u zwierząt dzikich, z czego 233 u lisów. Jak wykazują dane za lata 2004–2009, liczba przypadków wścieklizny na terytorium państwa uległa dalszemu, znacznemu zmniejszeniu (załączniki nr 1–6 do programu).
W ostatnich latach przypadki wścieklizny u zwierząt występują najczęściej na terenach położonych wzdłuż północno-wschodniej i wschodniej granicy Rzeczypospolitej Polskiej, gdzie zauważono przechodzenie zwierząt zakażonych wścieklizną z terenów Ukrainy oraz z terenów Federacji Rosyjskiej (obwód kaliningradzki).
Na przełomie 1991 r. i 1992 r. opracowano założenia do programu zwalczania wścieklizny w Rzeczypospolitej Polskiej.
W pierwszym etapie realizacji programu zwalczania wścieklizny wykładanie szczepionki przeciwko wściekliźnie miało objąć teren położony w pasie przygranicznym z Republiką Federalną Niemiec (Szczecin, Gorzów Wielkopolski, Zielona Góra, Jelenia Góra, Wałbrzych, Legnica, Opole, Wrocław, Poznań, Piła, Leszno, Koszalin), gdzie wścieklizna u lisów wystąpiła endemicznie i stwierdzano najczęściej przypadki tej choroby. Zaproponowano wykładanie szczepionki dwa razy w roku – wiosną i jesienią – po 16 dawek (przynęt) na km2. Wykładanie szczepionki miało być przeprowadzane ręcznie. Stopniowo akcja miała być rozszerzana o kolejne województwa w kierunku wschodnim. Wraz z wykładaniem szczepionki miała być prowadzona kontrola szczepień określająca wskaźnik przyjęcia szczepionki przez lisy oraz wskaźnik nabytej odporności.
Jednak w 1992 r. zmieniono sposób rozrzucania szczepionki z ręcznego na wyrzucanie z samolotów, a liczbę województw objętych szczepieniem zmieniono z 12 do 6. Odstąpiono od rozrzucania szczepionki w ówczesnych województwach: opolskim, wrocławskim, leszczyńskim, pilskim, poznańskim, koszalińskim.
Ostatecznie na terytorium Rzeczypospolitej Polskiej rozpoczęto program szczepień lisów przeciwko wściekliźnie w 1993 r.
W 1994 r. obszar szczepień został powiększony o 6 ówczesnych województw: koszalińskie, słupskie, pilskie, katowickie, bielskie, skierniewickie.
W 1995 r. obszar szczepień został powiększony o kolejne 10 ówczesnych województw: gdańskie, bydgoskie, konińskie, leszczyńskie, poznańskie, kaliskie, wrocławskie, opolskie, częstochowskie, warszawskie.
W 1996 r. obszar szczepień został powiększony o dalsze 4 ówczesne województwa: krośnieńskie, nowosądeckie, elbląskie, piotrkowskie.
W 1997 r. obszar szczepień został powiększony o województwo krakowskie.
W 1998 r. obszar szczepień został powiększony o kolejnych 5 województw: tarnowskie, sieradzkie, radomskie, łódzkie, lubelskie – 1 gmina.
W 1999 r. zmieniony został podział administracyjny państwa z 49 województw na 16 województw i wówczas szczepieniami objęto całkowicie województwa: dolnośląskie, lubuskie, zachodniopomorskie, wielkopolskie, śląskie, pomorskie, opolskie, małopolskie, natomiast częściowo województwa: kujawsko-pomorskie, lubelskie, łódzkie, warmińsko-mazurskie, mazowieckie, podkarpackie. Natomiast w województwie podlaskim i świętokrzyskim nie prowadzono szczepień.
W 2000 r. obszar szczepień nie uległ zmianie. W wyniku gwałtownego wzrostu zachorowań zwierząt na wściekliznę na terenach, gdzie nie prowadzono szczepień lisów przeciwko wściekliźnie, oraz na granicy „obszaru szczepionego” z „obszarem nieszczepionym” w 2001 r. wprowadzono zmodernizowany program szczepień lisów wolno żyjących przeciwko wściekliźnie, w którym zrezygnowano w akcji wiosennej ze szczepień w zachodniej części terytorium Rzeczypospolitej Polskiej, gdzie od dłuższego czasu nie odnotowywano przypadków wścieklizny u zwierząt. Obszar objęty szczepieniami to:
1) w województwie zachodniopomorskim powiat wałecki;
2) w województwie dolnośląskim powiaty: dzierżoniowski, ząbkowicki i kłodzki;
3) w województwie mazowieckim powiaty: warszawski zachodni, gostyniński, sochaczewski, żyrardowski, grodziski, pruszkowski, piaseczyński, grójecki, białobrzeski, przysuski, radomski, szydłowiecki, zwoleński, lipski, kozienicki, sierpecki, płoński, nowodworski, ciechanowski, mławski, żuromiński, przasnyski, ostrołęcki, makowski, legionowski i pułtuski;
4) w województwie lubelskim gmina Janowiec i część gminy Puławy;
5) w województwie podkarpackim powiaty: bieszczadzki, brzozowski, dębicki, jasielski, kolbuszowski, krośnieński, łańcucki, mielecki, ropczycki, rzeszowski, sanocki, strzyżowski i tarnobrzeski w całości oraz powiat jarosławski, leżajski, niżański, przemyski, przeworski i stalowowolski w części na południe od linii rzeki San;
6) województwo warmińsko-mazurskie, kujawsko-pomorskie, wielkopolskie, małopolskie, opolskie, śląskie, łódzkie, świętokrzyskie;
7) województwo pomorskie, z wyjątkiem powiatów: słupskiego, lęborskiego i bytowskiego.
Natomiast w akcji jesiennej 2001 r. szczepieniami objęto większość terytorium Rzeczypospolitej Polskiej, poza województwem podlaskim oraz częścią województw: lubelskiego i podkarpackiego.
Od 2002 r. akcja szczepień obejmuje całe terytorium Rzeczypospolitej Polskiej.
Tabela 1
Wyniki badań monitoringowych akcji szczepień
| Akcje szczepień | Obecność TC (%) | RFFIT (%) | Różnicowanie szczepów wirusa |
| jesień 1998 r. | 67,70 | 68,00 | 0 |
| wiosna 1999 r. | 64,30 | 66,70 | 0 |
| jesień 1999 r. | 64,40 | 82,90 | 0 |
| wiosna 2000 r. | 55,30 | 75,30 | 0 |
| jesień 2000 r. | 64,40 | 81,70 | 0 |
| wiosna i jesień 2001 r. | 52,40 | 62,10 | 0 |
| wiosna i jesień 2002 r. | 66,70 | 72,90 | 0 |
| wiosna i jesień 2003 r. | 78,40 | 92,60 | 0 |
| wiosna i jesień 2004 r. | 82,50 | 94,00 | 0 |
| wiosna i jesień 2005 r. | 85,56 | 83,60 | 0 |
| wiosna i jesień 2006 r. | 87,17 | 82,12 | 43 |
| wiosna i jesień 2007 r. | 83,17 | 80,21 | 42 |
| wiosna i jesień 2008 r. | 86,87 | 79,66 | 19 |
| wiosna i jesień 2009 r.* | 89,32 | 81,11 | 6 |
| * Na podstawie wstępnych wyników badań. | |||
3. Opis przedłożonego programu
Zgodnie z ustawą z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (Dz. U. z 2008 r. Nr 213, poz. 1342, z późn. zm.) wścieklizna należy do chorób zakaźnych zwierząt podlegających obowiązkowi zwalczania na terytorium Rzeczypospolitej Polskiej (załącznik nr 2 do ustawy).
Lisy wolno żyjące na obszarach określonych przez ministra właściwego do spraw rolnictwa, zgodnie z art. 56 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, podlegają obowiązkowemu szczepieniu ochronnemu przeciwko wściekliźnie.
Na podstawie rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 2 czerwca 2004 r. w sprawie szczegółowych warunków i sposobu przeprowadzania ochronnych szczepień lisów wolno żyjących przeciwko wściekliźnie (Dz. U. Nr 142, poz. 1509) szczepienia ochronne lisów wolno żyjących przeprowadza wojewódzki lekarz weterynarii. Zgodnie z tym rozporządzeniem szczepionka jest rozrzucana z samolotu lub wykładana ręcznie dwa razy w ciągu roku kalendarzowego na obszarach lasów oraz we wszystkich miejscach bytowania lisów wolno żyjących. Szczepionka może być podana raz w roku, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono przypadków wystąpienia wścieklizny w okresie dwóch kolejnych lat. Natomiast szczepień ochronnych nie przeprowadza się, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono wścieklizny w okresie trzech kolejnych lat.
Liczba dawek szczepionki zależy od stopnia zalesienia i ukształtowania terenu, populacji zwierząt dzikich oraz przyjętego sposobu podania szczepionki, ale nie powinna być mniejsza niż 20 dawek na 1 km2 powierzchni.
Badania monitoringowe, wykonywane w celu określenia efektywności doustnych szczepień lisów wolno żyjących przeciwko wściekliźnie, przeprowadza się na podstawie rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 17 grudnia 2004 r. w sprawie określenia jednostek chorobowych, sposobu prowadzenia kontroli oraz zakresu badań kontrolnych zakażeń zwierząt (Dz. U. Nr 282, poz. 2813, z późn. zm.). Zgodnie z tym rozporządzeniem w celu kontroli wścieklizny pobiera się do badań tkankę mózgową, surowicę i żuchwę od 8 lisów odstrzelonych na każdych 100 km2 obszaru, na którym lisy wolno żyjące zostały objęte szczepieniem ochronnym przeciwko wściekliźnie. Natomiast w celu izolacji i określenia szczepu wirusa wścieklizny do badań przesyła się tkankę mózgową lisów wolno żyjących, u których w badaniu laboratoryjnym potwierdzono wściekliznę.
4. Środki przewidziane w programie
4.1. Skrócony opis środków przewidzianych w programie
Rok: 2011

4.2. Organizacja i nadzór nad realizacją programu
Zgodnie z art. 57 ust. 8 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt Główny Lekarz Weterynarii nadzoruje realizację programu zwalczania chorób zakaźnych zwierząt, a w przypadku programu współfinansowanego ze środków pochodzących z Unii Europejskiej – informuje Komisję Europejską o postępach w jego realizacji zgodnie z obowiązującymi przepisami Unii Europejskiej.
Organem odpowiedzialnym za nadzór i koordynację działań zapewniających realizację programu monitoringu i zwalczania wścieklizny jest na poziomie krajowym Główny Lekarz Weterynarii.
Odpowiedzialność terenowych organów Inspekcji Weterynaryjnej za realizację programów została określona w ustawie z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej (Dz. U. z 2010 r. Nr 112, poz. 744, z późn. zm.) oraz w ustawie z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 23 grudnia 2010 r. w sprawie krajowych laboratoriów referencyjnych (Dz. U. z 2011 r. Nr 8, poz. 38) wyznaczyło Zakład Wirusologii Państwowego Instytutu Weterynaryjnego – Państwowego Instytutu Badawczego (PIW-PIB) w Puławach jako krajowe laboratorium referencyjne dla wścieklizny.
Zgodnie z § 2 ust. 1 rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 2 czerwca 2004 r. w sprawie szczegółowych warunków i sposobu przeprowadzania ochronnych szczepień lisów wolno żyjących przeciwko wściekliźnie szczepienia ochronne lisów wolno żyjących przeprowadzają wojewódzcy lekarze weterynarii. Diagnostyka wścieklizny przy wystąpieniu podejrzenia tej jednostki chorobowej jest przeprowadzana przez 16 zakładów higieny weterynaryjnej (ZHW): we Wrocławiu, w Bydgoszczy, Lublinie, Gorzowie Wielkopolskim, Łodzi, Krakowie, Warszawie, Opolu, Krośnie, Białymstoku, Gdańsku, Katowicach, Kielcach, Olsztynie, Poznaniu, Szczecinie oraz przez krajowe laboratorium referencyjne PIW-PIB w Puławach – przy użyciu immunofluorescencji odcisków mózgowych z monowalentnym koniugatem antynukleokapsydowym. Ponadto badania izolacji wirusa na myszach wykonywane są przez 8 ZHW: we Wrocławiu, w Bydgoszczy, Lublinie, Gorzowie Wielkopolskim, Krakowie, Krośnie, Białymstoku i Szczecinie. Natomiast badania izolacji wirusa na kulturach komórkowych neuroblastomy wykonuje się w ZHW w Opolu oraz Poznaniu, a także w krajowym laboratorium referencyjnym PIW-PIB w Puławach. Genotypizację izolatów wirusa wścieklizny przeprowadza wyłącznie krajowe laboratorium referencyjne PIW-PIB w Puławach.
Badania monitoringowe w celu sprawdzenia skuteczności szczepienia lisów wolno żyjących przeprowadza się przy zastosowaniu:
1) immunofluorescencji odcisków mózgowych – badanie w kierunku wścieklizny w 16 ZHW: we Wrocławiu, w Bydgoszczy, Lublinie, Gorzowie Wielkopolskim, Łodzi, Krakowie, Warszawie, Opolu, Krośnie, Białymstoku, Gdańsku, Katowicach, Kielcach, Olsztynie, Poznaniu, Szczecinie oraz w krajowym laboratorium referencyjnym PIW-PIB w Puławach;
2) szlifów kostnych żuchwy – badania na obecność markera (TC – tetracykliny) w 6 ZHW: w Opolu, Ostrołęce, Bydgoszczy, Łodzi, Krośnie i Poznaniu oraz w krajowym laboratorium referencyjnym PIW-PIB w Puławach;
3) testu seroneutralizacji (RFFIT) – określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep z serca lub płyn z klatki piersiowej) w 3 ZHW: w Opolu, Ostrołęce, Bydgoszczy oraz w krajowym laboratorium referencyjnym PIW-PIB w Puławach;
4) zbierania i analizowania danych epidemiologicznych na temat zdiagnozowanych przypadków wścieklizny na obszarze objętym szczepieniem.
4.3. Opis regionów administracyjnych, na których program ma być wdrożony
Terytorium Rzeczypospolitej Polskiej
| Województwo | Całkowita powierzchnia województwa (km2) | Powierzchnia objęta doustnym szczepieniem lisów wolno żyjących przeciwko wściekliźnie (km2) |
| 1 | 2 | 3 |
| dolnośląskie | 19 947,00 | 15 958,00 |
| kujawsko-pomorskie | 17 972,00 | 16 533,40 |
| lubelskie | 25 122,00 | 22 441,00 |
| lubuskie | 13 988,00 | 13 054,00 |
| łódzkie | 18 219,00 | 16 970,00 |
| małopolskie | 15 183,00 | 15 183,00 |
| mazowieckie | 35 558,00 | 32 069,00 |
| opolskie | 9 412,00 | 8 000,00 |
| podkarpackie | 17 845,00 | 16 133,00 |
| podlaskie | 20 187,00 | 18 162,00 |
| 1 | 2 | 3 |
| pomorskie | 18 310,00 | 16 559,00 |
| śląskie | 12 334,00 | 10 130,50 |
| świętokrzyskie | 11 710,00 | 10 500,00 |
| warmińsko-mazurskie | 24 173,00 | 21 483,00 |
| wielkopolskie | 29 827,00 | 27 637,66 |
| zachodniopomorskie | 22 892,00 | 20 000,00 |
| Razem | 312 679,00 | 280 813,56 |
4.4. Opis środków przewidzianych w programie
4.4.1. Powiadomienie o chorobie
Zgodnie z ustawą z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (załącznik nr 2 do ustawy) wścieklizna należy do chorób zakaźnych zwierząt podlegających obowiązkowi zwalczania na terytorium Rzeczypospolitej Polskiej.
Zgodnie z art. 42 tej ustawy w przypadku podejrzenia wystąpienia choroby zakaźnej zwierząt obowiązek niezwłocznego zawiadomienia organu Inspekcji Weterynaryjnej albo najbliższego podmiotu świadczącego usługi z zakresu medycyny weterynaryjnej, albo wójta (burmistrza, prezydenta miasta) dotyczy wszystkich osób mających kontakt ze zwierzętami, w szczególności w związku z wykonywaniem obowiązków służbowych lub zawodowych. Wójt (burmistrz, prezydent miasta) niezwłocznie informuje organ Inspekcji Weterynaryjnej o otrzymaniu ww. zawiadomienia. Podmiot świadczący usługi z zakresu medycyny weterynaryjnej niezwłocznie informuje organ Inspekcji Weterynaryjnej, jeżeli na podstawie otrzymanego zawiadomienia podejrzewa wystąpienie choroby zakaźnej zwierząt podlegającej obowiązkowi zwalczania.
4.4.2. Zwierzęta i populacja zwierząt objęte programem
Programem jest objęta populacja lisów wolno żyjących na terytorium Rzeczypospolitej Polskiej.
Metoda obliczania populacji: statystyki myśliwskie, wskaźnik nocnego liczenia, liczenie lisich jam
| Region | Szacunki liczebności populacji lisów wolno żyjących | |||
| 2006 r. | 2007 r. | 2008 r. | 2009 r. | |
| terytorium Rzeczypospolitej Polskiej | 204 064 | 202 740 | 209 500 | 203 300 |
| Razem | 204 064 | 202 740 | 209 500 | 203 300 |
4.4.3. Zastosowane badania i plany pobierania próbek
Badania i analizy używane do diagnostyki wścieklizny i nadzoru nad programem szczepień:
1) badania serologiczne: test seroneutralizacji (RFFIT) – zgodnie z Podręcznikiem OIE (rozdział 2.1.13. B.2.b) – wykonywany przez ZHW w Opolu, Ostrołęce i Bydgoszczy, wyznaczone do przeprowadzania badań monitoringowych określających efektywność szczepień doustnych lisów wolno żyjących przeciwko wściekliźnie, oraz przez krajowe laboratorium referencyjne dla wścieklizny PIW-PIB w Puławach;
2) badania wirusologiczne i immunochemiczne:
a) immunofluorescencja odcisków mózgowych z monowalentnym koniugatem antynukleokapsydowym (FAT fluorescent antibody test) – zgodnie z Podręcznikiem OIE (rozdział 2.1.13 B.1.c.i) – test w kierunku wścieklizny wykonywany przez 16 ZHW,
b) różnicowanie szczepów wirusa wścieklizny – badanie wykonywane jedynie przez krajowe laboratorium referencyjne PIW-PIB w Puławach,
c) izolacja wirusa:
– izolacja wirusa na myszach – zgodnie z Podręcznikiem OIE (rozdział 2.1.13 B.1.c.ii) – wykonywana przez 8 ZHW: we Wrocławiu, Bydgoszczy, Lublinie, Gorzowie Wielkopolskim, Krakowie, Krośnie, Białymstoku i Szczecinie,
– izolacja wirusa wścieklizny w hodowli komórek mysiej neuroblastomy – zgodnie z Podręcznikiem OIE (rozdział 2.1.13 B.1.c.ii) – wykonywana jedynie przez krajowe laboratorium referencyjne PIW-PIB w Puławach oraz przez ZHW w Opolu i Poznaniu;
3) inne badania to szlify kostne żuchwy – badanie na obecność markera (TC) – wykonywane przez 6 ZHW: w Opolu, Ostrołęce, Bydgoszczy, Łodzi, Krośnie i Poznaniu, wyznaczonych do przeprowadzania testów monitoringowych w celu określenia poziomu podjęcia szczepionki przez lisy wolno żyjące, oraz przez krajowe laboratorium referencyjne PIW-PIB w Puławach;
4) monitoring szczepień w Rzeczypospolitej Polskiej obejmuje przeprowadzenie następujących badań:
a) test seroneutralizacji (RFFIT) w celu określenia poziomu uodpornienia lisów wolno żyjących, a tym samym efektywności szczepień doustnych, wykonywany przez 3 wyznaczone ZHW: w Bydgoszczy, Ostrołęce i Opolu oraz przez krajowe laboratorium referencyjne PIW-PIB w Puławach,
b) badanie na obecność markera (TC) w celu określenia poziomu podjęcia szczepionki przez lisy wolno żyjące, wykonywane przez 6 wyznaczonych ZHW: w Opolu, Ostrołęce, Bydgoszczy, Łodzi, Krośnie i Poznaniu oraz przez krajowe laboratorium referencyjne PIW-PIB w Puławach,
c) różnicowanie szczepów wirusa wścieklizny w celu rozróżnienia terenowych szczepów wirusa od szczepów szczepionkowych, wykonywane przez krajowe laboratorium referencyjne PIW-PIB w Puławach.
Badania monitoringowe (RFFIT, TC), wykonywane w celu określenia efektywności doustnych szczepień lisów wolno żyjących przeciwko wściekliźnie, przeprowadza się zgodnie z rozporządzeniem Ministra Rolnictwa i Rozwoju Wsi z dnia 17 grudnia 2004 r. w sprawie określenia jednostek chorobowych, sposobu prowadzenia kontroli oraz zakresu badań kontrolnych zakażeń zwierząt. Zgodnie z tym rozporządzeniem w celu kontroli wścieklizny pobiera się do badań tkankę mózgową, surowicę i żuchwę od 8 lisów odstrzelonych na każdych 100 km2 obszaru, na którym lisy zostały objęte szczepieniem ochronnym przeciwko wściekliźnie. Natomiast w celu izolacji i określenia szczepu wirusa wścieklizny do badań przesyła się tkankę mózgową lisów wolno żyjących, u których badaniem laboratoryjnym potwierdzono wściekliznę.
Badania monitoringowe (RFFIT, TC) wykonywane w celu określenia efektywności doustnych szczepień lisów wolno żyjących przeciwko wściekliźnie
| Województwo | Całkowita powierzchnia województwa (km2) | Powierzchnia objęta programem szczepień (km2) | Całkowita powierzchnia bytowania lisów wolno żyjących na terenie województwa, z którego lisy powinny zostać odstrzelone i dostarczone do badań monitoringowych (km2) | Liczba lisów, która powinna zostać odstrzelona w ramach programu monitoringu, w ciągu roku |
| 1 | 2 | 3 | 4 | 5 |
| dolnośląskie | 19 947,00 | 15 958,00 | 15 410,35 | 1 233 |
| kujawsko-pomorskie | 17 972,00 | 16 533,40 | 16 132,28 | 1 291 |
| lubelskie | 25 122,00 | 22 441,00 | 22 441,00 | 1 795 |
| lubuskie | 13 988,00 | 13 054,00 | 12 108,00 | 969 |
| łódzkie | 18 219,00 | 16 970,00 | 16 970,00 | 1 358 |
| małopolskie | 15 183,00 | 15 183,00 | 15 183,00 | 1 215 |
| mazowieckie | 35 558,00 | 32 069,00 | 32 069,00 | 2 566 |
| opolskie | 9 412,00 | 8 000,00 | 8 000,00 | 640 |
| podkarpackie | 17 845,00 | 16 133,00 | 16 133,00 | 1 291 |
| podlaskie | 20 187,00 | 18 162,00 | 14 687,00 | 1 175 |
| pomorskie | 18 310,00 | 16 559,00 | 15 424,00 | 1 234 |
| śląskie | 12 334,00 | 10 130,50 | 10 042,00 | 803 |
| świętokrzyskie | 11 710,00 | 10 500,00 | 10 500,00 | 840 |
| warmińsko-mazurskie | 24 173,00 | 21 483,00 | 21 483,00 | 1 719 |
| wielkopolskie | 29 827,00 | 27 637,66 | 27 637,66 | 2 211 |
| zachodniopomorskie | 22 892,00 | 20 000,00 | 16 018,26 | 1 281 |
| Razem | 312 679,00 | 280 813,56 | 270 238,55 | 21 621 |
| Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Rodzaj badania | Populacja docelowa | Rodzaj próbki | Cel | Liczba planowanych badań |
| terytorium Rzeczypospolitej Polskiej | RFFIT | lisy wolno żyjące | surowica | kontrola szczepień, monitoring akcji | 21 621 |
| terytorium Rzeczypospolitej Polskiej | test na obecność markera (TC) | lisy wolno żyjące | żuchwa | kontrola szczepień, monitoring akcji | 21 621 |
| Razem | 43 242 | ||||
4.4.4. Zastosowane szczepionki i programy szczepień
Stosowane szczepionki: zgodne z wytycznymi Światowej Organizacji Zdrowia Zwierząt (OIE), Światowej Organizacji Zdrowia (WHO) oraz standardami UE (Raport Komitetu Naukowego ds. Zdrowia Zwierząt i Ochrony Zwierząt przyjęty dnia 23 października 2002 r.), dopuszczone do stosowania w Polsce zgodnie z odrębnymi przepisami krajowymi. Szczepionkami obecnie zarejestrowanymi w Polsce są Fuchsoral (SAD B19) i Lysvulpen (SAD Bern). Jest dostępna także szczepionka Rabigen SAG2 (SAG2) zarejestrowana w EMEA. Szczepionki używane w akcji szczepień są wybierane corocznie w trybie ustawy z dnia 29 stycznia 2004 r. – Prawo zamówień publicznych (Dz. U. z 2010 r. Nr 113, poz. 759, z późn. zm.). Oferty na zakup szczepionki są składane na początku roku w każdym województwie. Szczepionka jest poddawana badaniu, w celu kontroli jakości, w kierunku określenia miana wirusa.
Na podstawie rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 2 czerwca 2004 r. w sprawie szczegółowych warunków i sposobu przeprowadzania ochronnych szczepień lisów wolno żyjących przeciwko wściekliźnie szczepienia ochronne lisów wolno żyjących przeprowadza wojewódzki lekarz weterynarii. Zgodnie z tym rozporządzeniem szczepionka jest rozrzucana z samolotu lub wykładana ręcznie dwa razy w ciągu roku kalendarzowego na obszarach lasów oraz we wszystkich miejscach bytowania lisów wolno żyjących. Szczepionka może być podana raz w roku, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono przypadków wystąpienia wścieklizny w okresie dwóch kolejnych lat. Natomiast szczepień ochronnych nie przeprowadza się, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono wścieklizny w okresie trzech kolejnych lat.
Liczba dawek szczepionki zależy od stopnia zalesienia i ukształtowania terenu, populacji zwierząt dzikich oraz przyjętego sposobu podania szczepionki, ale nie powinna być mniejsza niż 20 dawek na 1 km2 powierzchni.
4.4.5. Środki podejmowane w przypadku uzyskania dodatniego wyniku badania laboratoryjnego
Zgodnie z ustawą z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt oraz rozporządzeniem Ministra Rolnictwa i Rozwoju Wsi z dnia 7 stycznia 2005 r. w sprawie zwalczania wścieklizny (Dz. U. Nr 13, poz. 103), w przypadku stwierdzenia choroby powiatowy lekarz weterynarii wyznacza ognisko choroby oraz obejmuje je nadzorem, a także niezwłocznie powiadamia państwowego powiatowego inspektora sanitarnego o wyznaczeniu ogniska choroby oraz wyznacza obszar zagrożony wokół ogniska choroby.
Powiatowy lekarz weterynarii podejmuje również pozostałe czynności, zgodnie z przepisami rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 7 stycznia 2005 r. w sprawie zwalczania wścieklizny.
4.4.6. Kontrola wdrażania programu i sprawozdawczość
Zgodnie z art. 57 ust. 8 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt Główny Lekarz Weterynarii nadzoruje realizację programu zwalczania chorób zakaźnych zwierząt, a w przypadku programu współfinansowanego ze środków Unii Europejskiej – informuje Komisję Europejską o postępach w jego realizacji zgodnie z przepisami Unii Europejskiej.
5. Korzyści programu
Celem programu jest spadek liczby przypadków wścieklizny u zwierząt dzikich.
6. Dane epidemiologiczne dotyczące rozwoju choroby w ciągu ostatnich pięciu lat
6.1. Dane rozwarstwione dotyczące nadzoru i przeprowadzonych badań laboratoryjnych
| Rok: 2005 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne: RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek* | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 13 936 | 83,60% | 24 456 | 84 | 20 038 | 85,56% |
| Razem | 13 936 | 83,60% | 24 456 | 84 | 20 038 | 85,56% |
| * W tym 258 próbek przebadano również testem izolacji wirusa na myszach. | ||||||
Opis zastosowanych badań serologicznych: badanie serologiczne – test seroneutralizacji – RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny (badanie w ramach monitoringu oraz badanie przy wystąpieniu podejrzenia tej jednostki chorobowej).
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (tetracykliny).
| Rok: 2006 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne: RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek* | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 14 155 | 82,12% | 23 257 | 43 | 20 572 | 87,17% |
| Razem | 14 155 | 82,12% | 23 257 | 43 | 20 572 | 87,17% |
| * W tym 198 próbek przebadano również testem izolacji wirusa na myszach. | ||||||
Opis zastosowanych badań serologicznych: badanie serologiczne – test seroneutralizacji – RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny (badanie w ramach monitoringu oraz badanie przy wystąpieniu podejrzenia tej jednostki chorobowej).
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (tetracykliny).
| Rok: 2007 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne: RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek* | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 13 592 | 80,21% | 22 055 | 42 | 19 217 | 83,17% |
| Razem | 13 592 | 80,21% | 22 055 | 42 | 19 217 | 83,17% |
| * W tym 182 próbki przebadano również testem izolacji wirusa na myszach oraz 5 próbek przebadano testem izolacji wirusa na kulturach komórkowych neuroblastomy. | ||||||
Opis zastosowanych badań serologicznych: badanie serologiczne – test seroneutralizacji – RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny (badanie w ramach monitoringu oraz przy wystąpieniu podejrzenia tej jednostki chorobowej).
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (tetracykliny).
| Rok: 2008 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne: RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek* | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 14 744 | 79,66% | 21 293 | 19 | 19 788 | 86,87% |
| Razem | 14 744 | 79,66% | 21 293 | 19 | 19 788 | 86,87% |
| * W tym 117 próbek przebadano również testem izolacji wirusa na myszach oraz 10 próbek przebadano testem izolacji wirusa na kulturach komórkowych neuroblastomy. | ||||||
Opis zastosowanych badań serologicznych: badanie serologiczne – test seroneutralizacji – RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny (badanie w ramach monitoringu oraz badanie przy wystąpieniu podejrzenia tej jednostki chorobowej).
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (tetracykliny).
| Rok: 2009 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne: RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek** | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 10 204* | 81,11% | 23 153 | 6 | 16 494 | 89,32% |
| Razem | 10 204* | 81,11% | 23 153 | 6 | 16 494 | 89,32% |
| * Na podstawie wstępnych wyników badań. ** W tym 107 próbek przebadano również testem izolacji wirusa na myszach oraz 7 próbek przebadano testem izolacji wirusa na kulturach komórkowych neuroblastomy. | ||||||
Opis zastosowanych badań serologicznych: badanie serologiczne – test seroneutralizacji – RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny (badanie w ramach monitoringu oraz przy wystąpieniu podejrzenia tej jednostki chorobowej).
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (tetracykliny).
6.2. Dane dotyczące zakażenia
| Rok: 2005 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 84 |
| Razem | – | 84 |
| Rok: 2005 | Choroba: wścieklizna | Gatunek zwierząt: inne gatunki wrażliwe |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 54 |
| Razem | – | 54 |
| Rok: 2006 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 43 |
| Razem | – | 43 |
| Rok: 2006 | Choroba: wścieklizna | Gatunek zwierząt: inne gatunki wrażliwe |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 39 |
| Razem | – | 39 |
| Rok: 2007 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 42 |
| Razem | – | 42 |
| Rok: 2007 | Choroba: wścieklizna | Gatunek zwierząt: inne gatunki wrażliwe |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 28 |
| Razem | – | 28 |
| Rok: 2008 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 19 |
| Razem | – | 19 |
| Rok: 2008 | Choroba: wścieklizna | Gatunek zwierząt: inne gatunki wrażliwe |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 10 |
| Razem | – | 10 |
| Rok: 2009 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 6 |
| Razem | – | 6 |
| Rok: 2009 | Choroba: wścieklizna | Gatunek zwierząt: inne gatunki wrażliwe |
| Region | Liczba zakażonych stad | Liczba zakażonych zwierząt |
| terytorium Rzeczypospolitej Polskiej | – | 2 |
| Razem | – | 2 |
6.3. Dane dotyczące programów szczepień lub leczenia
| Rok: 2004 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 11 269 876 | – | – |
| Razem | – | – | – | – | – | 11 269 876 | – | – |
| Rok: 2005 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 11 271 760 | – | – |
| Razem | – | – | – | – | – | 11 271 760 | – | – |
| Rok: 2006 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 12 906 008 | – | – |
| Razem | – | – | – | – | – | 12 906 008 | – | – |
| Rok: 2007 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 11 735 940 | – | – |
| Razem | – | – | – | – | – | 11 735 940 | – | – |
| Rok: 2008 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 11 713 553 | – | – |
| Razem | – | – | – | – | – | 11 713 553 | – | – |
| Rok: 2009 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 11 681 566 | – | – |
| Razem | – | – | – | – | – | 11 681 566 | – | – |
| Rok: 2010 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku* | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 11 269 876 | – | – |
| Razem | – | – | – | – | – | 11 269 876 | – | – |
| * Planowana do wyłożenia liczba dawek szczepionki. | ||||||||
| Rok: 2011 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Całkowita liczba stad | Całkowita liczba zwierząt | Informacja o programach szczepień lub leczenia | |||||
| liczba stad objętych programem szczepień lub leczenia | liczba stad zaszczepionych lub poddanych leczeniu | liczba zwierząt zaszczepionych lub poddanych leczeniu | liczba wyłożonych dawek szczepionki lub zastosowanych dawek leku* | liczba dorosłych zwierząt zaszczepionych | liczba młodych zwierząt zaszczepionych | |||
| terytorium Rzeczypospolitej Polskiej | – | – | – | – | – | 11 232 542 | – | – |
| Razem | – | – | – | – | – | 11 232 542 | – | – |
| * Planowana do wyłożenia liczba dawek szczepionki. | ||||||||
Opis stosowanych szczepień, działań terapeutycznych lub innych: wiosenna i jesienna akcja szczepień w 2011 r. obejmie terytorium Rzeczypospolitej Polskiej na obszarze 280 813,56 km2. Akcje będą prowadzone na tych samych zasadach co w latach poprzednich. Planuje się wyłożenie co najmniej 20 dawek szczepionki/km2. W sumie zostaną zastosowane 11 232 542 dawki szczepionki.
6.4. Dane dotyczące dzikiej zwierzyny
6.4.1. Oszacowanie liczebności populacji dzikiej zwierzyny
| Rok: 2005 | Metody szacowania: statystyki myśliwskie, wskaźnik nocnego liczenia, liczenie lisich jam |
| Region | Szacunki liczebności populacji danego gatunku zwierząt wolno żyjących | |||
| gatunek: lis wolno żyjący | gatunek: sarna | gatunek: jeleń | gatunek: dzik | |
| terytorium Rzeczypospolitej Polskiej | 186 737 | 620 980 | 109 960 | 152 393 |
| Razem | 186 737 | 620 980 | 109 960 | 152 393 |
| Rok: 2006 | Metody szacowania: statystyki myśliwskie, wskaźnik nocnego liczenia, liczenie lisich jam |
| Region | Szacunki liczebności populacji danego gatunku zwierząt wolno żyjących | |||
| gatunek: lis wolno żyjący | gatunek: sarna | gatunek: jeleń | gatunek: dzik | |
| terytorium Rzeczypospolitej Polskiej | 204 064 | 635 215 | 115 748 | 156 043 |
| Razem | 204 064 | 635 215 | 115 748 | 156 043 |
| Rok: 2007 | Metody szacowania: statystyki myśliwskie, wskaźnik nocnego liczenia, liczenie lisich jam |
| Region | Szacunki liczebności populacji danego gatunku zwierząt wolno żyjących | |||
| gatunek: lis wolno żyjący | gatunek: sarna | gatunek: jeleń | gatunek: dzik | |
| terytorium Rzeczypospolitej Polskiej | 202 740 | 646 006 | 123 038 | 159 268 |
| Razem | 202 740 | 646 006 | 123 038 | 159 268 |
| Rok: 2008 | Metody szacowania: statystyki myśliwskie, wskaźnik nocnego liczenia, liczenie lisich jam |
| Region | Szacunki liczebności populacji danego gatunku zwierząt wolno żyjących | |||
| gatunek: lis wolno żyjący | gatunek: sarna | gatunek: jeleń | gatunek: dzik | |
| terytorium Rzeczypospolitej Polskiej | 209 500 | 760 200 | 163 700 | 211 800 |
| Razem | 209 500 | 760 200 | 163 700 | 211 800 |
| Rok: 2009 | Metody szacowania: statystyki myśliwskie, wskaźnik nocnego liczenia, liczenie lisich jam |
| Region | Szacunki liczebności populacji danego gatunku zwierząt wolno żyjących | |||
| gatunek: lis wolno żyjący | gatunek: sarna | gatunek: jeleń | gatunek: dzik | |
| terytorium Rzeczypospolitej Polskiej | 203 300 | 827 500 | 176 100 | 251 000 |
| Razem | 203 300 | 827 500 | 176 100 | 251 000 |
6.4.2. Monitorowanie dzikiej zwierzyny
| Rok: 2005 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne – RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 13 936 | 83,60% | 20 636 | 84 | 20 038 | 85,56% |
| Razem | 13 936 | 83,60% | 20 636 | 84 | 20 038 | 85,56% |
Opis zastosowanych badań serologicznych: badanie serologiczne – test RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny.
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (TC – tetracykliny).
| Rok: 2006 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne – RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 14 155 | 82,12% | 21 418 | 43 | 20 572 | 87,17% |
| Razem | 14 155 | 82,12% | 21 418 | 43 | 20 572 | 87,17% |
Opis zastosowanych badań serologicznych: badanie serologiczne – test RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny.
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (TC – tetracykliny).
| Rok: 2007 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne – RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 13 592 | 80,21% | 20 296 | 42 | 19 217 | 83,17% |
| Razem | 13 592 | 80,21% | 20 296 | 42 | 19 217 | 83,17% |
Opis zastosowanych badań serologicznych: badanie serologiczne – test RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny.
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (TC – tetracykliny).
| Rok: 2008 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne – RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 14 744 | 79,66% | 20 166 | 19 | 19 788 | 86,87% |
| Razem | 14 744 | 79,66% | 20 166 | 19 | 19 788 | 86,87% |
Opis zastosowanych badań serologicznych: badanie serologiczne – test RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny.
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (TC – tetracykliny).
| Rok: 2009 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Badania serologiczne – RFFIT | Badania mikrobiologiczne lub wirusologiczne | Inne testy: TC | |||
| liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | liczba przebadanych próbek* | liczba próbek z dodatnim wynikiem | liczba przebadanych próbek | odsetek próbek z dodatnim wynikiem | |
| terytorium Rzeczypospolitej Polskiej | 10 204 | 81,11% | 20 308 | 6 | 16 494 | 89,32% |
| Razem | 10 204 | 81,11% | 20 308 | 6 | 16 494 | 89,32% |
| * Na podstawie wstępnych wyników badań. | ||||||
Opis zastosowanych badań serologicznych: badanie serologiczne – test RFFIT [określenie miana przeciwciał wirusa wścieklizny w surowicy (skrzep krwi z serca lub płyn z klatki piersiowej)].
Opis zastosowanych badań mikrobiologicznych lub wirusologicznych: immunofluorescencja odcisków mózgowych – badanie w kierunku wścieklizny.
Opis innych zastosowanych badań: szlify kości żuchwy – badanie na obecność markera (TC – tetracykliny).
6.4.3. Dane dotyczące szczepień lub leczenia dzikiej zwierzyny
| Rok: 2011 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region (województwo) | Powierzchnia (km2) | Program szczepienia lub leczenia | ||
| liczba dawek szczepionki lub produktu leczniczego, która zostanie wyłożona lub podana | liczba akcji | całkowita liczba dawek szczepionki lub produktu leczniczego, która zostanie wyłożona lub podana | ||
| dolnośląskie | 19 947,00* 15 958,00** | 638 320 | 2 (wiosenna i jesienna) | 638 320 |
| kujawsko-pomorskie | 17 972,00* 16 533,40** | 661 336 | 2 (wiosenna i jesienna) | 661 336 |
| lubelskie | 25 122,00* 22 441,00** | 897 640 | 2 (wiosenna i jesienna) | 897 640 |
| lubuskie | 13 988,00* 13 054,00** | 522 160 | 2 (wiosenna i jesienna) | 522 160 |
| łódzkie | 18 219,00* 16 970,00** | 678 800 | 2 (wiosenna i jesienna) | 678 800 |
| małopolskie | 15 183,00* 15 183,00** | 607 320 | 2 (wiosenna i jesienna) | 607 320 |
| mazowieckie | 35 558,00* 32 069,00** | 1 282 760 | 2 (wiosenna i jesienna) | 1 282 760 |
| opolskie | 9 412,00* 8 000,00** | 320 000 | 2 (wiosenna i jesienna) | 320 000 |
| podkarpackie | 17 845,00* 16 133,00** | 645 320 | 2 (wiosenna i jesienna) | 645 320 |
| podlaskie | 20 187,00* 18 162,00** | 726 480 | 2 (wiosenna i jesienna) | 726 480 |
| pomorskie | 18 310,00* 16 559,00** | 662 360 | 2 (wiosenna i jesienna) | 662 360 |
| śląskie | 12 334,00* 10 130,50** | 405 220 | 2 (wiosenna i jesienna) | 405 220 |
| świętokrzyskie | 11 710,00* 10 500,00** | 420 000 | 2 (wiosenna i jesienna) | 420 000 |
| warmińsko-mazurskie | 24 173,00* 21 483,00** | 859 320 | 2 (wiosenna i jesienna) | 859 320 |
| wielkopolskie | 29 827,00* 27 637,66** | 1 105 506 | 2 (wiosenna i jesienna) | 1 105 506 |
| zachodniopomorskie | 22 892,00* 20 000,00** | 800 000 | 2 (wiosenna i jesienna) | 800 000 |
| Razem | 312 679,00*** 280 813,56**** | 11 232 542 | 2 (wiosenna i jesienna) | 11 232 542 |
| * Całkowita powierzchnia województwa. ** Powierzchnia województwa objęta szczepieniem. *** Całkowita powierzchnia Rzeczypospolitej Polskiej. **** Powierzchnia Rzeczypospolitej Polskiej objęta programem szczepień. | ||||
Opis zastosowanego programu szczepień, terapeutycznego lub innego
Na podstawie rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 2 czerwca 2004 r. w sprawie szczegółowych warunków i sposobu przeprowadzania ochronnych szczepień lisów wolno żyjących przeciwko wściekliźnie szczepienia ochronne lisów wolno żyjących przeprowadza wojewódzki lekarz weterynarii. Zgodnie z ww. rozporządzeniem szczepionka jest rozrzucana z samolotu lub wykładana ręcznie dwa razy w ciągu roku kalendarzowego na obszarach lasów oraz we wszystkich miejscach bytowania lisów wolno żyjących. Szczepionka może być podana raz w roku, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono przypadków wystąpienia wścieklizny w okresie dwóch kolejnych lat. Natomiast szczepień ochronnych nie przeprowadza się, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono wścieklizny w okresie trzech kolejnych lat.
Liczba dawek szczepionki zależy od stopnia zalesienia i ukształtowania terenu, populacji zwierząt dzikich oraz przyjętego sposobu podania szczepionki, ale nie powinna być mniejsza niż 20 dawek na 1 km2 powierzchni.
7. Założenia programu
7.1. Założenia związane z badaniami
7.1.1. Założenia w zakresie badań diagnostycznych
| Rok: 2011 | Choroba: wścieklizna | Gatunek zwierząt: lisy wolno żyjące |
| Region | Rodzaj badania | Populacja docelowa | Rodzaj próbki | Cel | Liczba planowanych badań |
| terytorium Rzeczypospolitej Polskiej | immunofluorescencja odcisków mózgowych | lisy wolno żyjące | mózg | kontrola szczepień, monitoring akcji | 21 621 |
| terytorium Rzeczypospolitej Polskiej | RFFIT | lisy wolno żyjące | surowica | kontrola szczepień, monitoring akcji | 21 621 |
| terytorium Rzeczypospolitej Polskiej | test na obecność markera (TC) | lisy wolno żyjące | żuchwa | kontrola szczepień, monitoring akcji | 21 621 |
| Razem | 64 863 | ||||
7.1.2. Założenia w zakresie szczepień lub leczenia dzikiej zwierzyny
Na podstawie rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 2 czerwca 2004 r. w sprawie szczegółowych warunków i sposobu przeprowadzania ochronnych szczepień lisów wolno żyjących przeciwko wściekliźnie szczepienia ochronne lisów wolno żyjących przeprowadza wojewódzki lekarz weterynarii. Zgodnie z tym rozporządzeniem szczepionka jest rozrzucana z samolotu lub wykładana ręcznie dwa razy w ciągu roku kalendarzowego na obszarach lasów oraz we wszystkich miejscach bytowania lisów wolno żyjących. Szczepionka może być podana raz w roku, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono przypadków wystąpienia wścieklizny w okresie dwóch kolejnych lat. Natomiast szczepień ochronnych nie przeprowadza się, jeżeli na terenie województwa i na terenach województw graniczących z tym województwem nie stwierdzono wścieklizny w okresie trzech kolejnych lat.
Liczba dawek szczepionki zależy od stopnia zalesienia i ukształtowania terenu, populacji zwierząt dzikich oraz przyjętego sposobu podania szczepionki, ale nie powinna być mniejsza niż 20 dawek na 1 km2 powierzchni.
| Rok: 2011 | Choroba: wścieklizna | Gatunek zwierzęcia: lisy wolno żyjące |
| Region (województwo) | Powierzchnia (km2) | Cele programu szczepienia lub leczenia | ||
| liczba dawek szczepionki lub produktu leczniczego planowana do wyłożenia lub podania w ramach akcji | planowana liczba akcji | całkowita liczba dawek szczepionki lub produktu leczniczego planowana do wyłożenia lub podania | ||
| 1 | 2 | 3 | 4 | 5 |
| dolnośląskie | 19 947,00* 15 958,00** | 319 160 | 2 (wiosenna i jesienna) | 638 320 |
| kujawsko-pomorskie | 17 972,00* 16 533,40** | 330 668 | 2 (wiosenna i jesienna) | 661 336 |
| lubelskie | 25 122,00* 22 441,00** | 448 820 | 2 (wiosenna i jesienna) | 897 640 |
| lubuskie | 13 988,00* 13 054,00** | 261 080 | 2 (wiosenna i jesienna) | 522 160 |
| łódzkie | 18 219,00* 16 970,00** | 339 400 | 2 (wiosenna i jesienna) | 678 800 |
| małopolskie | 15 183,00* 15 183,00** | 303 660 | 2 (wiosenna i jesienna) | 607 320 |
| 1 | 2 | 3 | 4 | 5 |
| mazowieckie | 35 558,00* 32 069,00** | 641 380 | 2 (wiosenna i jesienna) | 1 282 760 |
| opolskie | 9 412,00* 8 000,00** | 160 000 | 2 (wiosenna i jesienna) | 320 000 |
| podkarpackie | 17 845,00* 16 133,00** | 322 660 | 2 (wiosenna i jesienna) | 645 320 |
| podlaskie | 20 187,00* 18 162,00** | 363 240 | 2 (wiosenna i jesienna) | 726 480 |
| pomorskie | 18 310,00* 16 559,00** | 331 180 | 2 (wiosenna i jesienna) | 662 360 |
| śląskie | 12 334,00* 10 130,50** | 202 610 | 2 (wiosenna i jesienna) | 405 220 |
| świętokrzyskie | 11 710,00* 10 500,00** | 210 000 | 2 (wiosenna i jesienna) | 420 000 |
| warmińsko-mazurskie | 24 173,00* 21 483,00** | 429 660 | 2 (wiosenna i jesienna) | 859 320 |
| wielkopolskie | 29 827,00* 27 637,66** | 552 753 | 2 (wiosenna i jesienna) | 1 105 506 |
| zachodniopomorskie | 22 892,00* 20 000,00** | 400 000 | 2 (wiosenna i jesienna) | 800 000 |
| Razem | 312 679,00*** 280 813,56**** | 5 616 271 | 2 (wiosenna i jesienna) | 11 232 542 |
| * Całkowita powierzchnia województwa. ** Powierzchnia województwa objęta szczepieniem. *** Całkowita powierzchnia Rzeczypospolitej Polskiej. **** Powierzchnia Rzeczypospolitej Polskiej objęta programem szczepień. | ||||
8. Szacunkowa analiza kosztów programu1)
| Koszty związane z | Wyszczególnienie | Ilość jednos-tek | Koszt jednostko-wy w zł | Kwota całkowita w zł* | Koszt jednostkowy w euro** | Kwota całkowita w euro* | Wniosek o dofinansowanie z funduszy Wspólnoty (tak/nie) |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 1. Badania laboratoryjne – w 2011 | |||||||
| 1.1. Koszty badań | test: RFFIT | 21 621 | 20,81 | 449 933,01 | 5,24 | 113 361,81 | tak |
| test: TC | 21 621 | 2,73 | 59 025,33 | 0,69 | 14 871,59 | tak | |
| test: różnicowanie szczepów wirusa wścieklizny | 30 | 150,00 | 4 500,00 | 37,79 | 1 133,79 | tak | |
| test: jakość szczepionki (kontrola serii) | 56 | 233,61 | 13 082,16 | 58,86 | 3 296,08 | tak | |
| test: immunofluorescencja odcisków mózgowych – badanie w ramach monitoringu | 21 621 | 20,22 | 437 176,62 | 5,09 | 110 147,80 | tak | |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
|
| test: immunofluorescencja odcisków mózgowych – badanie przy wystąpieniu podejrzenia wścieklizny | 1 443 | 20,22 | 29 177,46 | 5,09 | 7 351,34 | tak |
| test: izolacji wirusa na myszach | 149 | 1 009,84 | 150 466,16 | 254,43 | 37 910,34 | tak | |
| test: izolacji wirusa na kulturach komórkowych neuroblastomy | 7 | 352,46 | 2 467,22 | 88,80 | 621,62 | tak | |
| 1.2. Koszty pobierania próbek | dostarczenie lisów do badania | 21 621 | 35,00 | 756 735,00 | 8,82 | 190 661,37 | tak |
| dowóz próbek do laboratorium (do badań przy wystąpieniu podejrzenia wścieklizny oraz badań w ramach monitoringu) | 769 partii (po 30 lisów) x 160 km | 0,83 | 102 123,20 | 0,21 | 25 730,21 | nie | |
| Razem | 2 004 686,16 |
| 505 085,95 |
| |||
| 2. Szczepienie – w 2011 r. | |||||||
| 2.1. Zakup szczepionki |
| 11 232 542 | 1,86 | 20 892 528,12 | 0,47 | 5 263 927,47 | tak |
| 2.2. Koszty dystrybucji |
| 11 232 542 | 1,05 | 11 794 169,10 | 0,26 | 2 971 571,96 | tak |
| Razem (poz. 2.1 i 2.2) | 32 686 697,22 |
| 8 235 499,43 | tak | |||
| Razem | 34 691 383,38 |
| 8 740 585,38 | tak | |||
| 1) Nie wlicza się kosztów stałych. Wszystkie wartości podane bez VAT. * Są to szacunkowe koszty, które zostaną dostosowane do wielkości wydatków zaplanowanych na zwalczanie chorób zakaźnych zwierząt w ustawie budżetowej na rok 2011. ** Wyliczenie kosztów według średniego kursu NBP na dzień 3 lutego 2010 r. (1 euro = 3,9690 zł). | |||||||
Załączniki do programu zwalczania wścieklizny
Załącznik nr 1
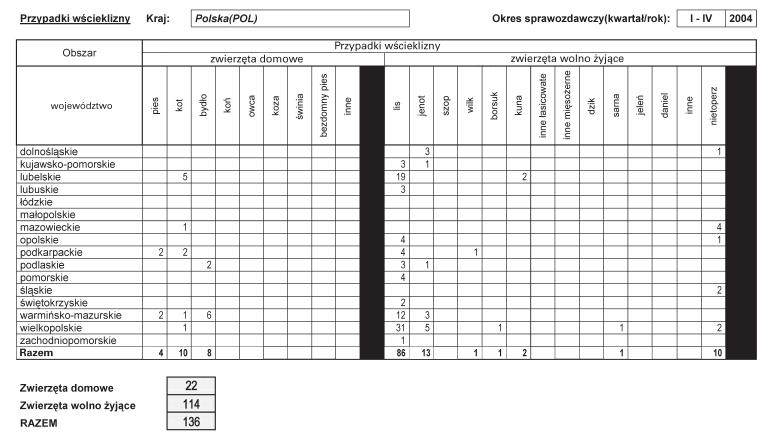
Załącznik nr 2
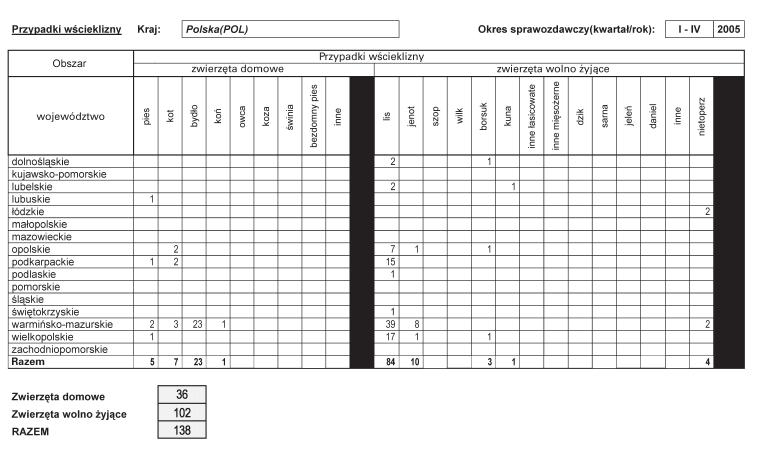
Załącznik nr 3
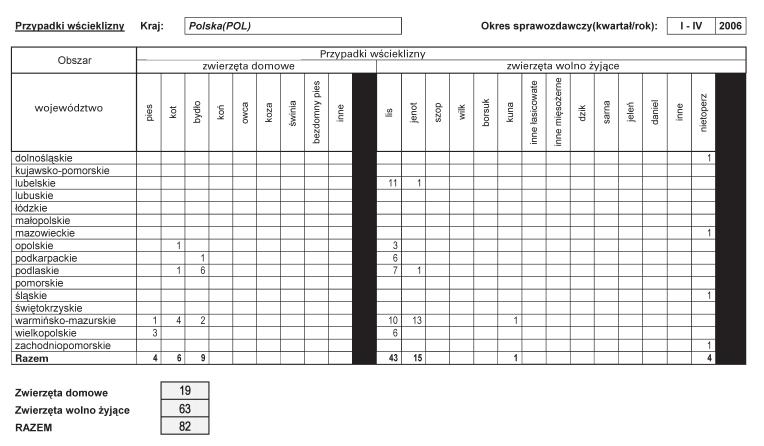
Załącznik nr 4
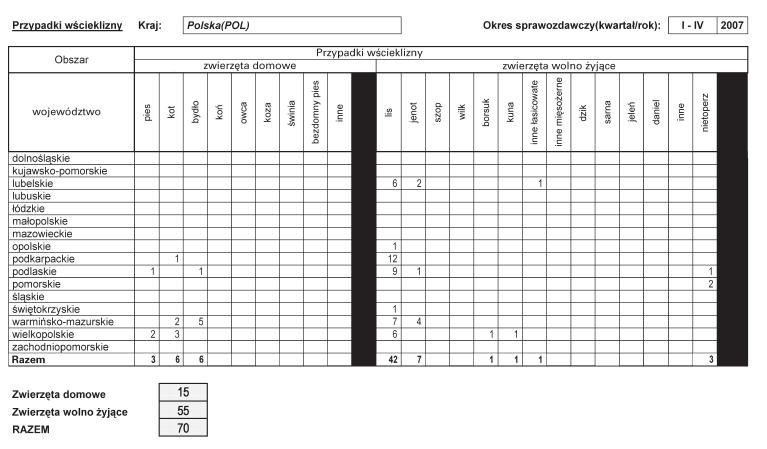
Załącznik nr 5
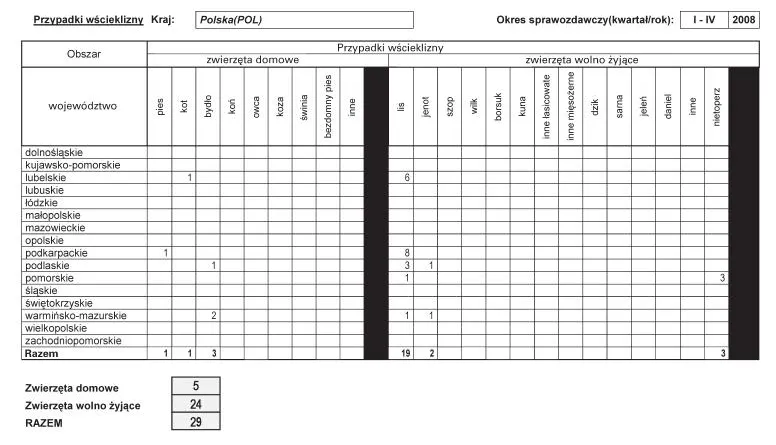
Załącznik nr 6
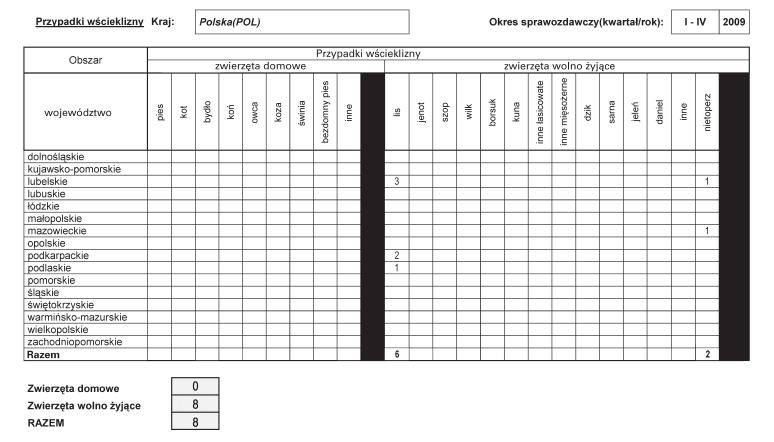
Załącznik nr 2
PROGRAM ZWALCZANIA GĄBCZASTEJ ENCEFALOPATII BYDŁA
(BOVINE SPONGIFORM ENCEPHALOPATHY – BSE)
1. Identyfikacja programu
Państwo członkowskie: Rzeczpospolita Polska
Choroba: Bovine spongiform encephalopathy (BSE)
Rok wdrażania: 2011
2. Opis programu
Celem realizacji programu jest wykrycie każdego przypadku gąbczastej encefalopatii bydła, zwanej dalej „BSE”, w populacji bydła w Rzeczypospolitej Polskiej. Wykrywanie jest pierwszym krokiem zapobiegającym przedostaniu się czynnika przenośnych gąbczastych encefalopatii przeżuwaczy, zwanych dalej „TSE”, do łańcucha pokarmowego ludzi i zwierząt.
Środki zapobiegawcze oraz zwalczanie polegają na usuwaniu zwierząt ze stad, w których stwierdzono przypadki BSE, poddaniu ubojowi kohorty oraz potomstwa, aktywnym nadzorze nad grupą bydła powyżej 30 miesiąca życia przeznaczonego do uboju w celu spożycia przez ludzi, bydła padłego oraz innych grup ryzyka bydła powyżej 24 miesiąca życia, zgodnie z rozporządzeniem Parlamentu Europejskiego i Rady (WE) nr 999/2001 z dnia 22 maja 2001 r. ustanawiającym zasady dotyczące zapobiegania, kontroli i zwalczania niektórych pasażowalnych gąbczastych encefalopatii (Dz. Urz. WE L 147 z 31.05.2001, str. 1, z późn. zm.; Polskie wydanie specjalne, rozdz. 3, t. 32, str. 289, z późn. zm.), zwanym dalej „rozporządzeniem nr 999/2001”.
3. Opis sytuacji epidemiologicznej choroby
Regularny monitoring BSE, zgodny z wymaganiami UE, rozpoczął się w listopadzie 2001 r. W pierwszych dwóch miesiącach monitoringu zbadano 30 309 sztuk bydła. Odpowiednio w 2002 r. zostało zbadanych 286 592, w 2003 r. – 455 413, w 2004 r. – 481 116, w 2005 r. – 515 976, w 2006 r. – 594 121, w 2007 r. – 603 810, w 2008 r. – 611 566, a w 2009 r. – 639 010 sztuk bydła.
Tabela 1.1
Dane z podziałem na grupy objęte monitoringiem
| Okres | Ubój bydła powyżej 30 mies. życia | Bydło poddane ubojowi z konieczności powyżej 24 mies. życia | Bydło poddane ubojowi sanitarnemu powyżej 24 mies. życia | Bydło padłe powyżej 24 mies. życia | Bydło podejrzane o chorobę | Ogółem |
| 2001 XI–XII | 29 882 | 347 | 0 | 80 | 0 | 30 309 |
| 2002 I–XII | 278 709 | 4 709 | 1 183 | 1 944 | 47 | 286 592 |
| 2003 I–XII | 428 452 | 9 401 | 2 757 | 14 715 | 88 | 455 413 |
| 2004 I–XII | 445 198 | 9 259 | 2 134 | 24 449 | 76 | 481 116 |
| 2005 I–XII | 472 028 | 10 495 | 648 | 32 552 | 253 | 515 976 |
| 2006 I–XII | 540 148 | 10 035 | 382 | 43 328 | 228 | 594 121 |
| 2007 I–XII | 546 243 | 9 529 | 61 | 47 883 | 94 | 603 810 |
| 2008 I–XII | 556 583 | 8 758 | 19 | 46 184 | 22 | 611 566 |
| 2009 I–XII | 587 339 | 6 811 | 9 | 43 958 | 13 | 638 133 |
Pierwszy przypadek BSE wykryto w drugim roku prowadzenia monitoringu (w 2002 r.). W tym też roku ogólna liczba wykrytych przypadków wyniosła 4.
W 2003 r. wykryto dalszych 5 przypadków, w 2004 r. obserwowano dalszy wzrost tej liczby; do końca 2004 r. wykryto 11 przypadków BSE. W 2005 r. wykryto ogółem 20 przypadków BSE, co stanowi największą roczną liczbę przypadków w Rzeczpospolitej Polskiej. W 2006 r. wykryto ogółem 10 przypadków, w 2007 r. wykryto 9 przypadków, w 2008 r. wykryto 5 przypadków, a w 2009 r. wykryto 4 przypadki.
Tabela 1.2
Zestawienie występowania przypadków BSE, z podziałem na lata oraz województwa
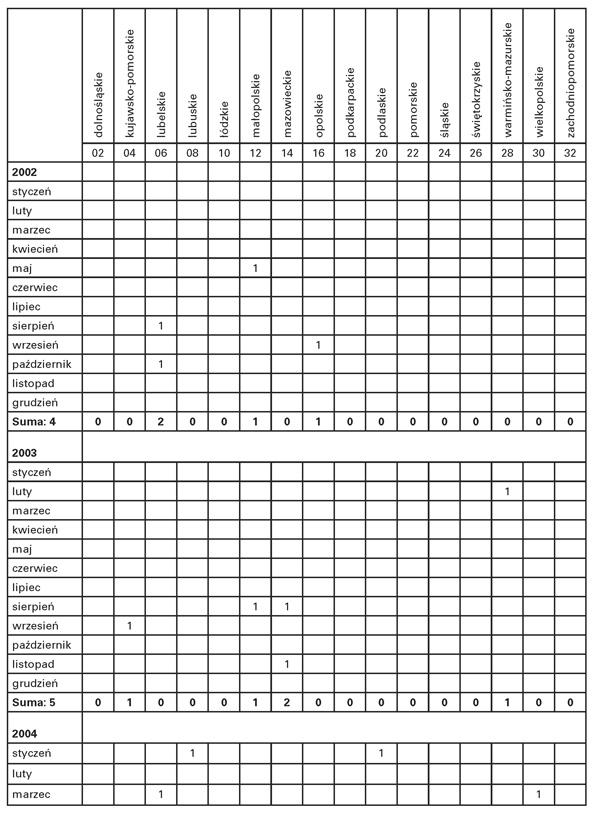
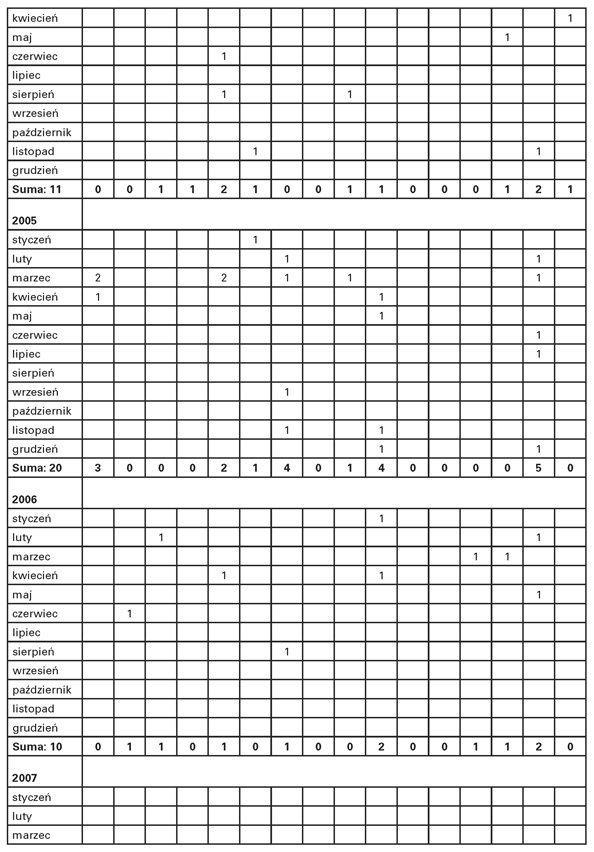
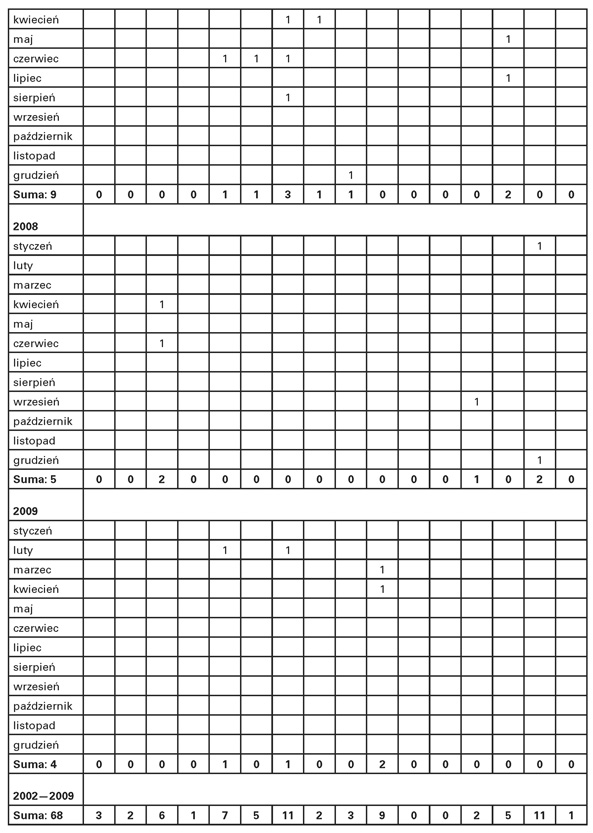
Największą liczbę przypadków wykryto w ramach tzw. „aktywnego nadzoru” w grupie zdrowego bydła kierowanego do normalnego uboju. W ramach „nadzoru pasywnego” wykryto zaledwie kilka przypadków BSE.
Tabela 1.3
Poszczególne grupy, w których stwierdzono przypadki BSE
| Rok | Liczba przypadków BSE | Poddane ubojowi jako zdrowe | Poddane ubojowi z konieczności | Z objawami klinicznymi | Padłe | Kohorta |
| 2002 | 4 | 3 | 0 | 1 | 0 | 0 |
| 2003 | 5 | 4 | 0 | 1 | 0 | 0 |
| 2004 | 11 | 8 | 2 | 0 | 1 | 0 |
| 2005 | 20 | 16 | 0 | 1 | 2 | 1 |
| 2006 | 10 | 7 | 0 | 0 | 3 | 0 |
| 2007 | 9 | 6 | 1 | 0 | 2 | 0 |
| 2008 | 5 | 4 | 1 | 0 | 0 | 0 |
| 2009 | 4 | 3 | 0 | 0 | 1 | 0 |
| Suma | 68 | 51 | 4 | 3 | 9 | 1 |
Wszystkie sztuki bydła, u których wykryto BSE, były polskiego pochodzenia. Dochodzenia epizootyczne prowadzone w celu wyjaśnienia dróg zakażeń wskazywały, iż najbardziej prawdopodobną drogą było zakażenie przez spożycie paszy zawierającej białko pochodzące od ssaków lub preparatów mlekozastępczych zawierających tłuszcz zwierzęcy.
W ostatnich 4 latach sytuacja w zakresie BSE stale podlegała zmianom, przy utrzymującej się przez pewien okres (2002–2005) tendencji wzrostowej. Wprowadzenie programu monitoringu, zgodnego z wytycznymi UE, pozwoliło na wykrycie zwierząt zakażonych. Od 2002 r. liczba tych przypadków systematycznie rosła i przedstawiała się następująco w okresie:
1) od 2002 do 2003 r. wzrost wynosił 25%;
2) od 2003 do 2004 r. wzrost wynosił 120%;
3) od 2004 do 2005 r. wzrost wynosił 82%.
W 2006 r. zaznaczyła się pierwsza tendencja spadkowa, liczba zakażeń osiągnęła poziom niższy niż w 2004 r.
Liczba przypadków BSE w latach 2002–2009, odzwierciedlająca tendencję wzrostową i spadkową
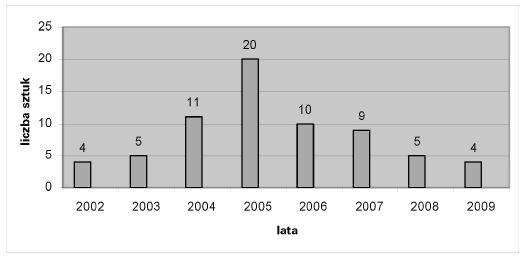
Biorąc pod uwagę wiek krów, u których stwierdzono BSE, można zauważyć, że najwyższą liczbę przypadków zaobserwowano u bydła urodzonego od 1994 do 2000 r. Najwyższy odsetek zakażeń dotyczy zwierząt urodzonych w 1996 r. i 1997 r. Najliczniej zakażoną grupę stanowi bydło w wieku od 5 do 9 roku życia.
Tabela 1.4
Zestawienie liczby przypadków BSE, w odniesieniu do roku urodzenia
| Rok urodzenia | Przypadki |
| 1990 | 1 |
| 1991 | 0 |
| 1992 | 3 |
| 1993 | 2 |
| 1994 | 4 |
| 1995 | 7 |
| 1996 | 11 |
| 1997 | 8 |
| 1998 | 5 |
| 1999 | 10 |
| 2000 | 7 |
| 2001 | 5 |
| 2002 | 0 |
| 2003 | 3 |
| 2004 | 1 |
| 2005 | 1 |
| SUMA | 68 |
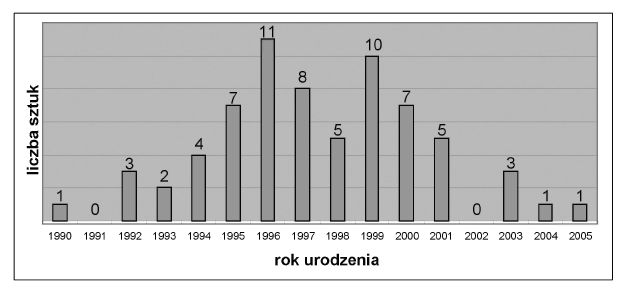
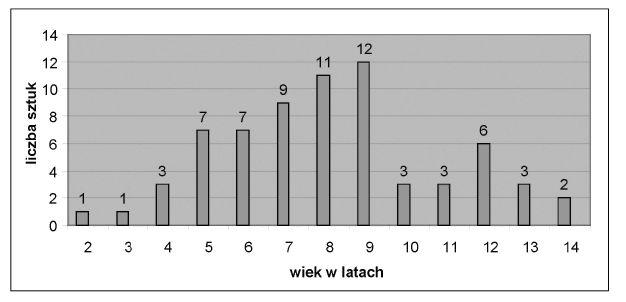
Tabela 1.5
Zestawienie liczby przypadków BSE, w odniesieniu do wieku zwierząt
| Wiek (lata) | Liczba sztuk |
| 2 | 1 |
| 3 | 1 |
| 4 | 3 |
| 5 | 7 |
| 6 | 7 |
| 7 | 9 |
| 8 | 11 |
| 9 | 12 |
| 10 | 3 |
| 11 | 3 |
| 12 | 6 |
| 13 | 3 |
| 14 | 2 |
| SUMA | 68 |
4. Środki przewidziane w programie
4.1. Władza centralna odpowiedzialna za nadzór i koordynację w województwach, na których obszarze będzie realizowany program
Za realizację programu będą odpowiedzialne organy Inspekcji Weterynaryjnej szczebla powiatowego i wojewódzkiego.
Zgodnie z art. 57 ust. 8 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (Dz. U. z 2008 r. Nr 213, poz. 1342, z późn. zm.) organ szczebla centralnego – Główny Lekarz Weterynarii – nadzoruje realizację programu zwalczania chorób zakaźnych zwierząt.
Ponadto, w przypadku programu współfinansowanego ze środków Unii Europejskiej, Główny Lekarz Weterynarii informuje Komisję Europejską o postępach w jego realizacji, zgodnie z przepisami obowiązującymi w Unii Europejskiej.
4.2. Opis i określenie obszarów geograficznych i administracyjnych, na których program będzie realizowany
Program monitorowania i zwalczania BSE jest i nadal będzie realizowany na całym terytorium Rzeczypospolitej Polskiej, gdzie działa 16 organów Inspekcji Weterynaryjnej szczebla wojewódzkiego (wojewódzcy lekarze weterynarii) oraz 305 organów Inspekcji Weterynaryjnej szczebla powiatowego (powiatowi lekarze weterynarii). Wojewódzki lekarz weterynarii kieruje działaniem Inspekcji Weterynaryjnej na obszarze województwa.
Rzeczpospolita Polska – podział na województwa
4.3. Regulacje prawne dotyczące rejestracji gospodarstw
Gospodarstwa w Rzeczypospolitej Polskiej są rejestrowane w Centralnej Bazie Danych Systemu Identyfikacji i Rejestracji Zwierząt (IRZ) prowadzonej przez Agencję Restrukturyzacji i Modernizacji Rolnictwa. Kwestię tę regulują następujące akty prawne:
1) ustawa z dnia 18 grudnia 2003 r. o krajowym systemie ewidencji producentów, ewidencji gospodarstw rolnych oraz ewidencji wniosków o przyznanie płatności (Dz. U. z 2004 r. Nr 10, poz. 76, z późn. zm.);
2) ustawa z dnia 2 kwietnia 2004 r. o systemie identyfikacji i rejestracji zwierząt (Dz. U. z 2008 r. Nr 204, poz. 1281, z późn. zm.);
3) ustawa z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Wymienione powyżej akty prawne określają szczegółowe zasady dotyczące identyfikacji i rejestracji zwierząt, gospodarstw oraz osób zajmujących się utrzymywaniem zwierząt gospodarskich.
4.4. Regulacje prawne dotyczące systemu identyfikacji i rejestracji zwierząt
Identyfikacja i rejestracja bydła w Rzeczypospolitej Polskiej są prowadzone zgodnie z:
1) ustawą z dnia 2 kwietnia 2004 r. o systemie identyfikacji i rejestracji zwierząt;
2) rozporządzeniem (WE) nr 1760/2000 Parlamentu Europejskiego i Rady z dnia 17 lipca 2000 r. ustanawiającym system identyfikacji i rejestracji bydła i dotyczącym etykietowania wołowiny i produktów z wołowiny oraz uchylającym rozporządzenie Rady (WE) nr 820/97 (Dz. Urz. WE L 204 z 11.08.2000, str. 1, z późn. zm.; Dz. Urz. Polskie wydanie specjalne, rozdz. 3, t. 30, str. 248, z późn. zm.);
3) rozporządzeniem Komisji nr 911/2004 z dnia 29 kwietnia 2004 r. w sprawie wykonania rozporządzenia (WE) nr 1760/2000 Parlamentu Europejskiego i Rady w zakresie kolczyków, paszportów i rejestrów gospodarstw (Dz. Urz. UE L 163 z 30.04.2004, str. 65, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 46, str. 242, z późn. zm.);
4) rozporządzeniem Komisji (WE) nr 494/98 z dnia 27 lutego 1998 r. ustanawiającym szczegółowe przepisy wykonawcze do rozporządzenia Rady (WE) nr 820/97 w odniesieniu do stosowania minimalnych sankcji administracyjnych w ramach systemu identyfikacji i rejestracji bydła (Dz. Urz. WE L 60 z 28.02.1998, str. 78, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 46, str. 12, z późn. zm.).
W Rzeczypospolitej Polskiej bydło podlega obowiązkowi oznakowania za pomocą pary kolczyków oraz podlega rejestracji w Centralnej Bazie Danych IRZ. Każdy kolczyk zawiera indywidualny numer rejestracyjny zwierzęcia oraz zakodowane inne dodatkowe informacje. Posiadacz bydła ma obowiązek oznakować za pomocą pary kolczyków nowo narodzone cielę niezwłocznie po urodzeniu i przesłać zgłoszenie o urodzeniu do Centralnej Bazy Danych. Na wykonanie tych czynności posiadacz ma 7 dni od dnia urodzenia zwierzęcia.
Wszystkie sztuki bydła są zaopatrzone w paszporty, które towarzyszą zwierzętom od urodzenia do śmierci. Wszystkie zdarzenia, w tym przemieszczenie z gospodarstwa do gospodarstwa, rzeźni, zakładu utylizacyjnego, padnięcie, powinny być zgłoszone do bazy danych.
Gospodarstwa są zarejestrowane w Centralnej Bazie Danych i każde z nich posiada indywidualny numer siedziby stada. W każdym gospodarstwie posiadacz bydła prowadzi rejestr stada. Wszystkie sztuki bydła znajdujące się w gospodarstwie muszą być wpisane do tego rejestru. Rejestr zawiera następujące informacje: datę urodzenia, zakupów, sprzedaży, padnięcia bydła.
Informacje o ww. zdarzeniach są przekazywane także do Centralnej Bazy Danych.
Wszystkie ww. środki są ustanowione zgodnie z zasadami określonymi w przepisach Unii Europejskiej, nie tylko ze względu na identyfikację i rejestrację zwierząt, ale także z powodów ochrony zdrowia zwierząt. Istniejący system, w przypadku wystąpienia choroby zakaźnej, może zostać użyty do śledzenia przemieszczeń zwierząt.
4.5. Regulacje prawne dotyczące obowiązku powiadamiania o BSE
W Rzeczypospolitej Polskiej BSE jest chorobą podlegającą obowiązkowi zgłaszania. Obowiązek ten wynika bezpośrednio z przepisów:
1) rozporządzenia Parlamentu Europejskiego i Rady (WE) nr 999/2001 z dnia 22 maja 2001 r. ustanawiającego zasady dotyczące zapobiegania, kontroli i zwalczania niektórych pasażowalnych gąbczastych encefalopatii;
2) ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Nie naruszając prawa wspólnotowego, w ww. ustawie określono obowiązek zgłaszania podejrzenia wystąpienia chorób zakaźnych zwierząt, w tym BSE.
Nie przewiduje się kar za zgłoszenie, w wyniku którego nie zostanie potwierdzona choroba. Nie przewiduje się również zwrotu kosztów przez osobę zgłaszającą podejrzenie, jeśli podejrzenie to nie potwierdzi się.
4.6. Monitorowanie bydła
Tabela 1.6
Przewidywana liczba badań bydła w kierunku BSE, które będą przeprowadzone w roku 2011
|
| Szacunkowa liczba badań |
| Zwierzęta określone w załączniku III – rozdział A część I pkt 2.1, pkt 3 i 4 rozporządzenia nr 999/2001 | 60 000 |
| Zwierzęta określone w załączniku III – rozdział A część I pkt 2.2 rozporządzenia nr 999/2001 | 580 000 |
| Inne: zwierzęta podejrzane o BSE | 60 |
| Suma badań: | 640 060 |
4.7. Regulacje prawne stanowiące podstawę do zwalczania BSE
4.7.1. Środki podejmowane w przypadku stwierdzenia BSE
Działania urzędowych lekarzy weterynarii związane z wystąpieniem przypadku BSE w Rzeczypospolitej Polskiej regulują następujące akty prawne:
1) rozporządzenie Parlamentu Europejskiego i Rady (WE) nr 999/2001 z dnia 22 maja 2001 r. ustanawiające zasady dotyczące zapobiegania, kontroli i zwalczania niektórych pasażowalnych gąbczastych encefalopatii;
2) ustawa z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
W przypadku otrzymania dodatniego wyniku, w zależności od sytuacji, są podejmowane w szczególności następujące środki:
1) wszystkie części tuszy zakażonego zwierzęcia są całkowicie niszczone;
2) wszystkie części tuszy zwierząt sąsiadujących z zakażoną tuszą na linii ubojowej (co najmniej jedna przed i dwie po) są całkowicie niszczone;
3) prowadzone jest dochodzenie epizootyczne.
Dochodzenie epizootyczne ma na celu:
1) określenie liczby i zidentyfikowanie wszystkich sztuk przeżuwaczy w gospodarstwie pochodzenia zwierzęcia zakażonego BSE;
2) ustalenie historii krów i miejsca pobytu potomstwa chorej krowy;
3) ustalenie kohorty dla tego przypadku;
4) ustalenie możliwej przyczyny choroby i drogi jej przeniesienia;
5) ustalenie innych zwierząt, zarówno przebywających w gospodarstwie, w którym stwierdzono chorobę, jak i przebywających w innych gospodarstwach, które mogły mieć kontakt z tym samym źródłem zakażenia BSE co zakażona krowa;
6) ustalenie przemieszczenia potencjalnie zakażonej paszy lub innych czynników mogących być przyczyną zakażenia w tym lub innym gospodarstwie.
Wszystkie zwierzęta, które zostały w trakcie dochodzenia uznane za potencjalnie zakażone, są zabijane, a produkty z nich pozyskane poddaje się unieszkodliwieniu.
4.7.2. Zwalczanie ogniska BSE
Przewidywana liczba zwierząt, które będą zabite w ramach zwalczania ogniska BSE, zgodnie z załącznikiem VII rozdział A pkt 2.1 do rozporządzenia nr 999/2001, wynosi 30 sztuk.
5. Koszty
5.1. Analiza kosztów
Ogólne oszacowanie kosztów programu monitoringu BSE na 2011 r. przewiduje wielkość wydatków na poziomie 12 801 200 zł, co przy przeliczeniu 1 euro = 3,9690 zł (według średniego kursu NBP na dzień 3 lutego 2010 r.) stanowi równowartość 3 225 296,04 euro. Do tego należy dodać koszt odszkodowań za bydło, przyznawanych na podstawie pkt 2 lit. a załącznika VII do rozporządzenia nr 999/2001, który szacunkowo wyniesie 105 000 zł, co stanowi równoważność 26 455,03 euro.
W okresie przygotowania kalkulacji koszt jednego badania wynosił około 20 zł, co stanowiło równowartość 5,04 euro.
Są to szacunkowe koszty, które zostaną dostosowane do wielkości wydatków przewidzianych na zwalczanie chorób zakaźnych zwierząt w ustawie budżetowej na rok 2011.
5.2. Szczegółowa analiza kosztów programu
| Lp. | Przeznaczenie kosztów | Wyszcze- | Liczba jednostek | Koszt jednostkowy w zł/euro | Ogółem kwota w zł | Ogółem kwota w euro | Wniosek o finanso- |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 1. | Badania w kierunku BSE1) |
|
|
|
|
|
|
| 1.1. | Szybkie badania | Test:2) | 640 060 | 20/5,04 | 12 801 200 | 3 225 296,04 | TAK |
| 2. | Testy na trzęsawkę owiec |
|
|
|
|
|
|
| 2.1. | Szybkie badania | Test: | N/A3) |
|
|
| NIE |
| 3. | Badania odróżniające |
|
|
|
|
|
|
| 3.1. | Wstępne badania molekularne | Test: | N/A |
|
|
| NIE |
| 4. | Określanie genotypów |
|
|
|
|
|
|
| 4.1. | Określenie genotypu zwierząt w ramach środków w zakresie monitorowania i zwalczania ustanowionych rozporządzeniem nr 999/2001 | Metoda: | N/A |
|
|
| NIE |
| 4.2. | Określenie genotypu zwierząt w ramach programu hodowlanego ustanowionego zgodnie z decyzją Komisji 2003/100/WE | Metoda: | N/A |
|
|
| NIE |
| 5. | Obowiązkowy ubój zwierząt |
|
|
|
|
|
|
| 5.1. | Odszkodowanie za bydło, które ma być zabite lub poddane ubojowi zgodnie z wymogami określonymi w rozporządzeniu nr 999/2001 w załączniku VII – rozdział A pkt 2.14) |
| 30 | 3 500/881,83 | 105 000 | 26 455,03 | TAK |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 5.2. | Odszkodowanie za owce i kozy, które mają być zabite lub poddane ubojowi zgodnie z wymogami określonymi w rozporządzeniu nr 999/2001 w załączniku VII – rozdział A pkt 2.1 |
| N/A |
|
|
|
|
| Ogółem w zł: | 12 906 200 | 3 251 751,07 |
| ||||
1) Określone w pkt 4.6.
2) Określone w pkt 4.6.
3) Dowolny spośród szybkich testów wymienionych w załączniku X do rozporządzenia nr 999/2001 w odniesieniu do bydła.
4) N/A – nie stosuje się.
Załącznik nr 3
PROGRAM MAJĄCY NA CELU WYKRYCIE WYSTĘPOWANIA ZAKAŻEŃ WIRUSAMI WYWOŁUJĄCYMI GRYPĘ PTAKÓW (AVIAN INFLUENZA) ORAZ POSZERZENIE WIEDZY NA TEMAT RYZYKA WYSTĄPIENIA TEJ CHOROBY
1. Identyfikacja programu
Państwo członkowskie: Rzeczpospolita Polska
Choroba: grypa ptaków (Avian influenza)
2. Realizacja programu u drobiu
2.1. Cele, ogólne wymogi i kryteria nadzoru
2.1.1. Cele
Obowiązek prowadzenia nadzoru w celu wykrycia występowania zakażeń wirusami grypy ptaków podtypami H5 i H7 u różnych gatunków drobiu wynika z art. 4 dyrektywy Rady 2005/94/WE z dnia 20 grudnia 2005 r. w sprawie wspólnotowych środków zwalczania grypy ptaków i uchylającej dyrektywę 92/40/EWG (Dz. Urz. UE L 10 z 14.01.2006, str. 16, z późn. zm.). Szczegółowe wytyczne w zakresie wdrażania tego nadzoru zostały określone w decyzji Komisji 2007/268/WE z dnia 13 kwietnia 2007 r. w sprawie wdrożenia programu nadzoru nad ptasią grypą u drobiu i dzikiego ptactwa w państwach członkowskich i zmieniającej decyzję 2004/450/WE (Dz. Urz. UE L 115 z 03.05.2007, str. 3, z późn. zm.).
Nadzór u drobiu obejmuje występowanie nisko zjadliwej grypy ptaków podtypów H5 lub H7.
Nadzór serologiczny nad nisko zjadliwą grypą ptaków podtypów H5 lub H7 u drobiu ma na celu:
1) wykrywanie bezobjawowych zakażeń nisko zjadliwą grypą ptaków podtypów H5 i H7, mając na uwadze wspomaganie systemów wczesnego wykrywania, a następnie zapobieganie możliwej mutacji tych wirusów w wysoce zjadliwą grypę ptaków;
2) wykrywanie zakażeń nisko zjadliwą grypą ptaków podtypów H5 i H7 u specjalnie wybranych populacji drobiu szczególnie narażonych na zakażenie z powodu systemu hodowli lub wrażliwości konkretnych gatunków;
3) wykazanie, że dane państwo, region lub dane gospodarstwo mają status wolny od grypy ptaków, która podlega zgłoszeniu w ramach międzynarodowego obrotu handlowego zgodnie z zasadami określonymi przez Światową Organizację Zdrowia Zwierząt (OIE).
2.1.2. Ogólne wymogi i kryteria
1. Pobieranie próbek w ramach programu trwa od dnia 1 stycznia do dnia 31 grudnia 2011 r.
W odniesieniu do drobiu pobieranie próbek dla każdej kategorii drobiu obejmuje okres odpowiadający jednemu z okresów produkcyjnych.
2. Próbki do badań pobiera powiatowy lekarz weterynarii oraz przesyła je do krajowego laboratorium referencyjnego ds. grypy ptaków w Państwowym Instytucie Weterynaryjnym – Państwowym Instytucie Badawczym (PIW-PIB) w Puławach.
3. Krajowe laboratorium referencyjne ds. grypy ptaków w PIW-PIB w Puławach przeprowadza badania próbek, a wyniki tych badań przekazuje właściwemu miejscowo powiatowemu lekarzowi weterynarii, Głównemu Lekarzowi Weterynarii oraz Wspólnotowemu Laboratorium Referencyjnemu ds. Grypy Ptaków.
4. Wykryte izolaty wirusów grypy ptaków krajowe laboratorium referencyjne ds. grypy ptaków w PIW-PIB w Puławach przekazuje Wspólnotowemu Laboratorium Referencyjnemu ds. Grypy Ptaków, zgodnie z prawem wspólnotowym, chyba że przyznane zostanie odstępstwo zgodnie z rozdziałem V ust. 4 Podręcznika diagnostycznego ustanowionego decyzją Komisji 2006/437/WE z dnia 4 sierpnia 2006 r. zatwierdzającej podręcznik diagnostyczny dotyczący grypy ptaków, przewidziany w dyrektywie Rady 2005/94/WE (Dz. Urz. UE L 237 z 31.08.2006, str. 1). Wirusy podtypu H5 lub H7 zostaną niezwłocznie przesłane i poddane standardowym charakterystykom (sekwencjonowanie nukleotydów/IVPI), zgodnie z Podręcznikiem diagnostycznym.
2.2. Koncepcja i wdrożenie programu dotyczącego drobiu
1. W gospodarstwach, gdzie stwierdzono pozytywne wyniki badań laboratoryjnych, przeprowadza się badania retrospektywne, a wnioski z tych badań krajowe laboratorium referencyjne ds. grypy ptaków w PIW-PIB w Puławach przedstawia Głównemu Lekarzowi Weterynarii, Komisji Europejskiej i Wspólnotowemu Laboratorium Referencyjnemu ds. Grypy Ptaków.
2. Dane dotyczące liczby próbek, które należy pobrać do badań na obszarze każdego z województw oraz w każdym z gospodarstw hodujących poszczególne kategorie drobiu, określono w tabelach 1–7 na podstawie analizy ryzyka, przeprowadzonej zgodnie z lit. B załącznika I do decyzji Komisji 2007/268/WE. Gospodarstwa zajmujące się hodowlą zwierzyny łownej lub ptaków bezgrzebieniowych zostały również uwzględnione w niniejszym programie.
Jeżeli w gospodarstwie znajduje się kilka kurników, należy odpowiednio zwiększyć liczbę próbek do badań serologicznych z takiego gospodarstwa i pobierać próbki od co najmniej pięciu ptaków z jednego kurnika.
Stada przyzagrodowe nie zostały uwzględnione w programie z uwagi na bardzo wysoką liczbę tych stad w relacji do liczby planowanych próbek.
3. Na podstawie oceny ryzyka na obszarze województwa, związanej z planowaniem pobierania próbek, wojewódzki lekarz weterynarii uwzględnia następujące elementy:
1) rodzaj produkcji (np. chów na wolnym wybiegu) i związane z nim ryzyko oraz uwzględnienie innych czynników, takich jak zróżnicowany wiek, wykorzystanie wód powierzchniowych, stosunkowo dłuższy okres życia, obecność więcej niż jednego gatunku w gospodarstwie lub inne ważne czynniki;
2) dostosowanie okresu pobierania próbek do innych określonych na poziomie lokalnym okresów, w których obecność innych gatunków drobiu w danym gospodarstwie mogłaby zwiększyć ryzyko wystąpienia choroby.
4. Próbki krwi do badań serologicznych od kaczek i gęsi powiatowy lekarz weterynarii pobiera, jeżeli to możliwe, od ptaków trzymanych na wybiegach.
Tabela 1
Gospodarstwa utrzymujące kury nioski reprodukcyjne
| Kod | Łączna liczba gospodarstwb) | Łączna liczba gospodarstw, z których pobiera się próbki | Szacunkowa liczba próbek na gospodarstwo | Szacunkowa łączna liczba badań, które zostaną wykonane zgodnie z daną metodą | Metody badania laboratoryjnego |
| PL11 | 38 | 3 | 10 | 60 | HI (H5/H7) |
| PL12 | 206 | 12 | 10 | 240 | HI (H5/H7) |
| PL21 | 17 | 2 | 10 | 40 | HI (H5/H7) |
| PL22 | 43 | 4 | 10 | 80 | HI (H5/H7) |
| PL31 | 14 | 2 | 10 | 40 | HI (H5/H7) |
| PL32 | 5 | 1 | 10 | 20 | HI (H5/H7) |
| PL33 | 38 | 3 | 10 | 60 | HI (H5/H7) |
| PL34 | 50 | 5 | 10 | 100 | HI (H5/H7) |
| PL41 | 52 | 5 | 10 | 100 | HI (H5/H7) |
| PL42 | 75 | 6 | 10 | 120 | HI (H5/H7) |
| PL43 | 9 | 1 | 10 | 20 | HI (H5/H7) |
| PL51 | 27 | 4 | 10 | 80 | HI (H5/H7) |
| PL52 | 48 | 5 | 10 | 100 | HI (H5/H7) |
| PL61 | 28 | 3 | 10 | 60 | HI (H5/H7) |
| PL62 | 11 | 1 | 10 | 20 | HI (H5/H7) |
| PL63 | 29 | 3 | 10 | 60 | HI (H5/H7) |
| SUMA | 690 | 60 | – | 1 200 | – |
Tabela 2
Gospodarstwa utrzymujące kury nioski towarowe
| Kod | Łączna liczba gospodarstwb) | Łączna liczba gospodarstw, z których pobiera się próbki | Szacunkowa liczba próbek na gospodarstwo | Szacunkowa łączna liczba badań, które zostaną wykonane zgodnie z daną metodą | Metody badania laboratoryjnego |
| PL11 | 52 | 3 | 10 | 60 | HI (H5/H7) |
| PL12 | 195 | 9 | 10 | 180 | HI (H5/H7) |
| PL21 | 95 | 5 | 10 | 100 | HI (H5/H7) |
| PL22 | 114 | 6 | 10 | 120 | HI (H5/H7) |
| PL31 | 38 | 2 | 10 | 40 | HI (H5/H7) |
| PL32 | 32 | 2 | 10 | 40 | HI (H5/H7) |
| PL33 | 29 | 2 | 10 | 40 | HI (H5/H7) |
| PL34 | 27 | 2 | 10 | 40 | HI (H5/H7) |
| PL41 | 192 | 9 | 10 | 180 | HI (H5/H7) |
| PL42 | 37 | 2 | 10 | 40 | HI (H5/H7) |
| PL43 | 52 | 3 | 10 | 60 | HI (H5/H7) |
| PL51 | 103 | 5 | 10 | 100 | HI (H5/H7) |
| PL52 | 31 | 2 | 10 | 40 | HI (H5/H7) |
| PL61 | 44 | 2 | 10 | 40 | HI (H5/H7) |
| PL62 | 51 | 3 | 10 | 60 | HI (H5/H7) |
| PL63 | 52 | 3 | 10 | 60 | HI (H5/H7) |
| SUMA | 1 144 | 60 | – | 1 200 | – |
Tabela 3
Gospodarstwa utrzymujące indyki rzeźne i reprodukcyjne
| Kod | Łączna liczba gospodarstwb) | Łączna liczba gospodarstw, z których pobiera się próbki | Szacunkowa liczba próbek na gospodarstwo | Szacunkowa łączna liczba badań, które zostaną wykonane zgodnie z daną metodą | Metody badania laboratoryjnego |
| PL11 | 39 | 5 | 10 | 100 | HI (H5/H7) |
| PL12 | 32 | 5 | 10 | 100 | HI (H5/H7) |
| PL21 | 10 | 2 | 10 | 40 | HI (H5/H7) |
| PL22 | 9 | 2 | 10 | 40 | HI (H5/H7) |
| PL31 | 35 | 5 | 10 | 100 | HI (H5/H7) |
| PL32 | 9 | 1 | 10 | 20 | HI (H5/H7) |
| PL33 | 7 | 1 | 10 | 20 | HI (H5/H7) |
| PL34 | 17 | 3 | 10 | 60 | HI (H5/H7) |
| PL41 | 67 | 8 | 10 | 160 | HI (H5/H7) |
| PL42 | 24 | 4 | 10 | 80 | HI (H5/H7) |
| PL43 | 119 | 10 | 10 | 200 | HI (H5/H7) |
| PL51 | 51 | 8 | 10 | 160 | HI (H5/H7) |
| PL52 | 3 | 1 | 10 | 20 | HI (H5/H7) |
| PL61 | 34 | 4 | 10 | 80 | HI (H5/H7) |
| PL62 | 375 | 26 | 10 | 520 | HI (H5/H7) |
| PL63 | 37 | 5 | 10 | 100 | HI (H5/H7) |
| SUMA | 868 | 90 | – | 1 800 | – |
Tabela 4
Gospodarstwa utrzymujące strusie
| Kod | Łączna liczba gospodarstwb) | Łączna liczba gospodarstw, z których pobiera się próbki | Szacunkowa liczba próbek na gospodarstwo | Szacunkowa łączna liczba badań, które zostaną wykonane zgodnie z daną metodą | Metody badania laboratoryjnego |
| PL11 | 11 | 4 | 5 | 40 | HI (H5/H7) |
| PL12 | 16 | 7 | 5 | 70 | HI (H5/H7) |
| PL21 | 3 | 1 | 5 | 10 | HI (H5/H7) |
| PL22 | 14 | 6 | 5 | 60 | HI (H5/H7) |
| PL31 | 2 | 1 | 5 | 10 | HI (H5/H7) |
| PL32 | 0 | 0 | 5 | 0 | HI (H5/H7) |
| PL33 | 0 | 0 | 5 | 0 | HI (H5/H7) |
| PL34 | 14 | 6 | 5 | 60 | HI (H5/H7) |
| PL41 | 14 | 6 | 5 | 60 | HI (H5/H7) |
| PL42 | 8 | 4 | 5 | 40 | HI (H5/H7) |
| PL43 | 13 | 5 | 5 | 50 | HI (H5/H7) |
| PL51 | 10 | 5 | 5 | 50 | HI (H5/H7) |
| PL52 | 1 | 1 | 5 | 10 | HI (H5/H7) |
| PL61 | 7 | 3 | 5 | 30 | HI (H5/H7) |
| PL62 | 4 | 2 | 5 | 20 | HI (H5/H7) |
| PL63 | 5 | 2 | 5 | 20 | HI (H5/H7) |
| SUMA | 122 | 53 | – | 530 | – |
Tabela 5
Gospodarstwa utrzymujące ptaki łowne
| Kod | Łączna liczba gospodarstwb) | Łączna liczba gospodarstw, z których pobiera się próbki | Szacunkowa liczba próbek na gospodarstwo | Szacunkowa łączna liczba badań, które zostaną wykonane zgodnie z daną metodą | Metody badania laboratoryjnego |
| PL11 | 6 | 4 | 10 | 80 | HI (H5/H7) |
| PL12 | 6 | 4 | 10 | 80 | HI (H5/H7) |
| PL21 | 1 | 1 | 10 | 20 | HI (H5/H7) |
| PL22 | 6 | 4 | 10 | 80 | HI (H5/H7) |
| PL31 | 3 | 1 | 10 | 20 | HI (H5/H7) |
| PL32 | 0 | 0 | 10 | 0 | HI (H5/H7) |
| PL33 | 2 | 1 | 10 | 20 | HI (H5/H7) |
| PL34 | 1 | 1 | 10 | 20 | HI (H5/H7) |
| PL41 | 8 | 5 | 10 | 100 | HI (H5/H7) |
| PL42 | 0 | 0 | 10 | 0 | HI (H5/H7) |
| PL43 | 12 | 9 | 10 | 180 | HI (H5/H7) |
| PL51 | 1 | 1 | 10 | 20 | HI (H5/H7) |
| PL52 | 7 | 4 | 10 | 80 | HI (H5/H7) |
| PL61 | 8 | 5 | 10 | 100 | HI (H5/H7) |
| PL62 | 1 | 1 | 10 | 20 | HI (H5/H7) |
| PL63 | 2 | 1 | 10 | 20 | HI (H5/H7) |
| SUMA | 64 | 42 | – | 840 | – |
Tabela 6
Gospodarstwa utrzymujące kaczki rzeźne i reprodukcyjne
| Kod | Łączna liczba gospodarstwb) | Łączna liczba gospodarstw, z których pobiera się próbki | Szacunkowa liczba próbek na gospodarstwo | Szacunkowa łączna liczba badań, które zostaną wykonane zgodnie z daną metodą | Metody badania laboratoryjnego |
| PL11 | 1 | 1 | 40 | 80 | HI (H5/H7) |
| PL12 | 5 | 2 | 40 | 160 | HI (H5/H7) |
| PL21 | 8 | 3 | 40 | 240 | HI (H5/H7) |
| PL22 | 3 | 1 | 40 | 80 | HI (H5/H7) |
| PL31 | 28 | 14 | 40 | 1 120 | HI (H5/H7) |
| PL32 | 29 | 14 | 40 | 1 120 | HI (H5/H7) |
| PL33 | 1 | 1 | 40 | 80 | HI (H5/H7) |
| PL34 | 0 | 0 | 40 | 0 | HI (H5/H7) |
| PL41 | 93 | 34 | 40 | 2 720 | HI (H5/H7) |
| PL42 | 4 | 1 | 40 | 80 | HI (H5/H7) |
| PL43 | 4 | 1 | 40 | 80 | HI (H5/H7) |
| PL51 | 4 | 1 | 40 | 80 | HI (H5/H7) |
| PL52 | 0 | 0 | 40 | 0 | HI (H5/H7) |
| PL61 | 10 | 4 | 40 | 320 | HI (H5/H7) |
| PL62 | 5 | 2 | 40 | 160 | HI (H5/H7) |
| PL63 | 2 | 1 | 40 | 80 | HI (H5/H7) |
| SUMA | 197 | 80 | – | 6 400 | – |
Tabela 7
Gospodarstwa utrzymujące gęsi rzeźne i reprodukcyjne
| Kod | Łączna liczba gospodarstwb) | Łączna liczba gospodarstw, z których pobiera się próbki | Szacunkowa liczba próbek na gospodarstwo | Szacunkowa łączna liczba badań, które zostaną wykonane zgodnie z daną metodą | Metody badania laboratoryjnego |
| PL11 | 60 | 7 | 40 | 560 | HI (H5/H7) |
| PL12 | 68 | 7 | 40 | 560 | HI (H5/H7) |
| PL21 | 11 | 2 | 40 | 160 | HI (H5/H7) |
| PL22 | 14 | 2 | 40 | 160 | HI (H5/H7) |
| PL31 | 161 | 11 | 40 | 880 | HI (H5/H7) |
| PL32 | 18 | 2 | 40 | 160 | HI (H5/H7) |
| PL33 | 91 | 8 | 40 | 640 | HI (H5/H7) |
| PL34 | 58 | 6 | 40 | 480 | HI (H5/H7) |
| PL41 | 314 | 19 | 40 | 1 520 | HI (H5/H7) |
| PL42 | 17 | 2 | 40 | 160 | HI (H5/H7) |
| PL43 | 53 | 6 | 40 | 480 | HI (H5/H7) |
| PL51 | 16 | 2 | 40 | 160 | HI (H5/H7) |
| PL52 | 10 | 2 | 40 | 160 | HI (H5/H7) |
| PL61 | 83 | 7 | 40 | 560 | HI (H5/H7) |
| PL62 | 59 | 6 | 40 | 480 | HI (H5/H7) |
| PL63 | 7 | 1 | 40 | 80 | HI (H5/H7) |
| SUMA | 1 040 | 90 | – | 7 200 | – |
Objaśnienia do tabel 1–7:
* Kod NUTS(2) – ang. Nomenclature of Units for Territorial Statistics – standard geokodowania przyjęty w Unii Europejskiej na potrzeby identyfikowania statystycznych jednostek terytorialnych, gdzie poszczególne kody oznaczają odpowiednio: PL51 – woj. dolnośląskie, PL61 – woj. kujawsko-pomorskie, PL31 – woj. lubelskie, PL43 – woj. lubuskie, PL11 – woj. łódzkie, PL21 – woj. małopolskie, PL12 – woj. mazowieckie, PL52 – woj. opolskie, PL32 – woj. podkarpackie, PL34 – woj. podlaskie, PL63 – woj. pomorskie, PL22 – woj. śląskie, PL33 – woj. świętokrzyskie, PL62 – woj. warmińsko-mazurskie, PL41 – woj. wielkopolskie, PL42 – woj. zachodniopomorskie.
a) Położenie gospodarstwa pochodzenia. Jeżeli nie można użyć kodu NUTS(2), należy określić położenie w stopniach długości i szerokości geograficznej.
b) Łączna liczba gospodarstw jednej kategorii drobiu w danym regionie NUTS(2).
2.3. Opis zastosowanych badań laboratoryjnych
1. Procedury pobierania próbek oraz badania laboratoryjne przeprowadza się zgodnie z Podręcznikiem diagnostycznym dotyczącym grypy ptaków (decyzja Komisji 2006/437/WE). Badania w kierunku grypy ptaków przeprowadza się w krajowym laboratorium referencyjnym ds. grypy ptaków w PIW-PIB w Puławach.
2. Wszystkie pozytywne wyniki serologiczne są potwierdzane w krajowym laboratorium referencyjnym ds. grypy ptaków w PIW-PIB w Puławach metodą hamowania hemaglutynacji, z użyciem wyznaczonych szczepów dostarczonych przez Wspólnotowe Laboratorium Referencyjne ds. Grypy Ptaków, przy czym wykonuje się:
1) dla H5:
a) wstępne badanie z użyciem szczepu teal/England/7894/06 (H5N3),
b) badanie wszystkich dodatnich próbek za pomocą szczepu chicken/Scotland/59 (H5N1) celem wyeliminowania przeciwciał reagujących krzyżowo z N3;
2) dla H7:
a) wstępne badanie z użyciem szczepu Turkey/England/647/77 (H7N7),
b) badanie wszystkich dodatnich próbek za pomocą szczepu African Starling/983/79 (H7N1) celem wyeliminowania przeciwciał reagujących krzyżowo z N7.
3. Opis programu dotyczącego dzikiego ptactwa
3.1. Cele, ogólne wymogi i kryteria nadzoru
3.1.1. Cele
Obowiązek prowadzenia nadzoru w celu poszerzenia wiedzy na temat zagrożeń pochodzących od dzikich ptaków związanych z wszelkimi występującymi u ptaków wirusami grypy ptaków wynika z art. 4 dyrektywy Rady 2005/94/WE z dnia 20 grudnia 2005 r. w sprawie wspólnotowych środków zwalczania grypy ptaków i uchylającej dyrektywę 92/40/EWG. Szczegółowe wytyczne w zakresie wdrażania tego nadzoru zostały określone w decyzji Komisji 2007/268/WE z dnia 13 kwietnia 2007 r. w sprawie wdrożenia programu nadzoru nad ptasią grypą u drobiu i dzikiego ptactwa w państwach członkowskich i zmieniającej decyzję 2004/450/WE.
Realizacja programu dotyczącego dzikiego ptactwa obejmuje występowanie wirusów wysoce zjadliwej grypy ptaków oraz nisko zjadliwej grypy ptaków.
Nadzór wirusologiczny nad grypą ptaków dzikiego ptactwa służy określeniu ryzyka wprowadzenia wirusów grypy ptaków (nisko i wysoce zjadliwej) do drobiu domowego przez:
1) zapewnienie wczesnego wykrywania wysoce zjadliwej grypy ptaków podtypu H5N1, w drodze badania wzrostu zachorowalności lub śmiertelności wśród dzikiego ptactwa;
2) prowadzenie obserwacji i badań żywego i padłego dzikiego ptactwa w przypadku wykrycia u niego wysoce zjadliwej grypy ptaków podtypu H5N1;
3) kontynuację obserwacji i badań różnych gatunków ptaków wędrownych żyjących na wolności, jako części ciągłego monitorowania wirusów nisko zjadliwej grypy ptaków. Próbki pobiera się głównie od ptactwa z rzędu blaszkodziobych (ptactwo wodne) i siewkowych (ptactwo brzegowe i mewy), aby ocenić, czy są one nosicielami wirusa nisko zjadliwej grypy ptaków podtypu H5 i H7 (badanie to również wykryłoby, jeżeli występują, wirusy wysoce zjadliwej grypy ptaków podtypu H5N1 i inne wirusy wysoce zjadliwej grypy ptaków). Badaniu należy poddać zwłaszcza gatunki o podwyższonym ryzyku związanym z grypą ptaków, wymienione w tabeli 8 programu.
Tabela 8
Gatunki o podwyższonym ryzyku związanym z grypą ptaków*
| Nazwa zwyczajowa | Nazwa naukowa |
| Łabędź czarnodzioby | Cygnus columbianus |
| Łabędź krzykliwy | Cygnus cygnus |
| Łabędź niemy | Cygnus olor |
| Gęsi | |
| Gęś krótkodzioba | Anser brachyrhynchus |
| Gęś zbożowa | Anser fabalis |
| Gęś białoczelna (europejska rasa) | Anser albifrons albifrons |
| Gęś mała | Anser erythropus |
| Gęś gęgawa | Anser anser |
| Bernikla białolica | Branta leucopsis |
| Bernikla obrożna | Branta bernicla |
| Bernikla rdzawoszyja | Branta ruficollis |
| Bernikla kanadyjska | Branta canadensis |
| Kaczki | |
| Świstun | Anas penelope |
| Cyraneczka | Anas crecca |
| Krzyżówka | Anas platyrhynchos |
| Rożeniec | Anas acuta |
| Cyranka | Anas querquedula |
| Płaskonos | Anas clypeata |
| Marmurka | Marmaronetta angustirostris |
| Hełmiatka | Netta rufina |
| Głowienka | Aythya ferina |
| Czernica | Aythya fuligula |
| Ptaki siewkowe | |
| Czajka | Vanellus vanellus |
| Siewka złota | Pluvialis apricaria |
| Rycyk | Limosa limosa |
| Batalion | Philomachus pugnax |
| Mewy | |
| Mewa śmieszka | Larus ridibundus |
| Mewa pospolita | Larus canus |
* Wykaz nie jest wyczerpujący i służy jedynie wskazaniu gatunków wędrownych, które mogą stanowić wysokie ryzyko wprowadzenia grypy ptaków do Wspólnoty, na podstawie ich tras wędrówek obejmujących obszary, na których u dzikiego ptactwa lub drobiu wystąpiła wysoce zjadliwa grypa ptaków H5N1. Wykaz ten opracowano na podstawie opinii naukowej na temat ptaków wędrownych i ich prawdopodobnej roli w rozprzestrzenianiu wysoce zjadliwej grypy ptaków, przyjętej dnia 12 maja 2006 r. przez Panel ds. zdrowia i dobrostanu zwierząt Europejskiego Urzędu ds. Bezpieczeństwa Żywności (EFSA), a także na podstawie prac przeprowadzonych przez Komitet ORNIS i wykonawców usług zleconych przez Dyrekcję Generalną ds. Środowiska Komisji Europejskiej. Aktualizacja tego wykazu jest możliwa po udostępnieniu wyników dalszych badań naukowych i na podstawie oceny ryzyka przeprowadzonej przez organy krajowe z uwzględnieniem konkretnej sytuacji ornitologicznej.
U dzikiego ptactwa nie stosuje się badań serologicznych, gdyż na ich podstawie nie można rozróżnić wysoce i nisko zjadliwych szczepów wirusa, a stwierdzenie obecności przeciwciał nie umożliwia określenia miejsca zarażenia dzikiego ptactwa. Metody te umożliwiają jednak rozróżnienie, u których gatunków ptaków (osiadłych lub wędrownych) występuje zakażenie wirusami H5/H7 lub wirusy te występują endemicznie.
3.1.2. Ogólne wymogi i kryteria
1. Pobieranie próbek będzie miało miejsce od dnia 1 stycznia do dnia 31 grudnia 2011 r.
2. Próbki do badań pobiera powiatowy lekarz weterynarii oraz przesyła je do krajowego laboratorium referencyjnego ds. grypy ptaków w PIW-PIB w Puławach.
3. Krajowe laboratorium referencyjne ds. grypy ptaków w PIW-PIB w Puławach przeprowadza badania próbek, a wyniki tych badań przekazuje właściwemu miejscowo powiatowemu lekarzowi weterynarii, Głównemu Lekarzowi Weterynarii oraz Wspólnotowemu Laboratorium Referencyjnemu ds. Grypy Ptaków.
4. Wykryte izolaty wirusów grypy ptaków występujące u dzikiego ptactwa krajowe laboratorium referencyjne ds. grypy ptaków w PIW-PIB w Puławach przekazuje do Wspólnotowego Laboratorium Referencyjnego ds. Grypy Ptaków zgodnie z prawem wspólnotowym, chyba że przyznane zostanie odstępstwo zgodnie z rozdziałem V ust. 4 Podręcznika diagnostycznego ustanowionego decyzją Komisji 2006/437/WE. Wirusy podtypu H5 lub H7 niezwłocznie przesyła się i poddaje standardowym charakterystykom (sekwencjonowanie nukleotydów/IVPI), zgodnie z Podręcznikiem diagnostycznym.
3.2. Koncepcja i wdrożenie programu dotyczącego dzikiego ptactwa
3.2.1. Koncepcja programu dotyczącego dzikiego ptactwa
Do celów opracowania programu dotyczącego dzikiego ptactwa przy określeniu gatunków i optymalizacji pobierania próbek organy Inspekcji Weterynaryjnej współpracują z epidemiologami, ornitologami i organami właściwymi ds. ochrony przyrody, a także z instytucjami zajmującymi się ochroną lub obserwacją ptaków oraz ze stacjami obrączkowania.
Pobieranie próbek od żywych ptaków dzikich objętych ochroną gatunkową ścisłą lub częściową wymaga uzyskania zezwolenia Generalnego Dyrektora Ochrony Środowiska lub właściwego miejscowo regionalnego dyrektora ochrony środowiska.
Przy wyborze badanych gatunków na obszarze powiatu powiatowy lekarz weterynarii uwzględnia sytuację pod względem dominacji gatunków oraz wielkości populacji ptaków. Podczas pobierania próbek należy uwzględnić sezonowość wędrówek, sposoby zachowania się gatunków ptaków, jeżeli dotyczy tras wędrówek, główne siedliska, instynkt stadny i mieszanie się podczas przelotu, a także wyniki programów realizowanych w latach 2003–2008.
W odniesieniu do wysoce zjadliwej grypy ptaków H5N1 należy uwzględnić wszystkie czynniki, aby móc określić prawdopodobieństwo narażenia dzikiego ptactwa na zarażenie się od zakażonego drobiu i dzikich ptaków na obszarach wystąpienia tej choroby oraz prawdopodobieństwo kontaktu dzikiego ptactwa z drobiem domowym w wybiegowych systemach hodowli drobiu.
1. Nadzór bierny nad chorym i padłym dzikim ptactwem obejmuje przede wszystkim:
1) obszary, na których występuje wzrost zachorowalności lub śmiertelności wśród dzikiego ptactwa;
2) obszary w pobliżu morza, jezior i wód, na których znaleziono padłe ptaki, a zwłaszcza jeżeli obszary znajdują się w pobliżu gospodarstw utrzymujących drób;
3) ptaki należące do gatunków o podwyższonym ryzyku związanym z grypą ptaków oraz inne dzikie ptactwo żyjące w ich bezpośrednim sąsiedztwie.
2. Nadzór czynny nad żywymi i klinicznie zdrowymi lub klinicznie chorymi, zranionymi lub upolowanymi ptakami koncentruje się na:
1) ptakach wędrownych z rzędu blaszkodziobych (ptactwo wodne) i siewkowych (ptactwo brzegowe i mewy);
2) obszarach zidentyfikowanych pod względem występowania dużej liczby ptaków wędrownych, na których dochodzi do mieszania się różnych gatunków tych ptaków, a zwłaszcza na obszarach w pobliżu gospodarstw drobiu;
3) wyborze gatunków o podwyższonym ryzyku związanym z grypą ptaków.
3. Badania żywego i padłego dzikiego ptactwa na obszarach, gdzie wykryto przypadki H5N1 (nadzór czynny i bierny), koncentrują się na:
1) dzikim ptactwie w celu wykrycia nosicieli bezobjawowych;
2) ptakach na obszarach, na których istnieją związki epidemiologiczne z wykrytymi przypadkami;
3) ptakach, które mogą mieć bezpośrednią styczność z hodowlą drobiu (obszar zapowietrzony, obszar zagrożony i obszar B) i które mogłyby być „nosicielami pośrednimi”.
Tabela 9
Liczba próbek, które należy pobrać od dzikiego ptactwa
| KOD NUTS (2)a) | Dzikie ptactwo, od którego pobiera się próbki | Liczba próbek, które zostaną pobrane w ramach czynnego nadzoru | Liczba próbek, które zostaną pobrane w ramach biernego nadzoru |
| PL11 |
| 50 |
|
| PL12 | 150 | ||
| PL21 | 50 | ||
| PL22 | 50 | ||
| PL31 | 50 | ||
| PL32 | 50 | ||
| PL33 | 40 | ||
| PL34 | 110 | ||
| PL41 | 80 | ||
| PL42 | 250 | ||
| PL43 | 230 | ||
| PL51 | 170 | ||
| PL52 | 50 | ||
| PL61 | 70 | ||
| PL62 | 170 | ||
| PL63 | 230 | ||
| SUMA |
| 1 800 | około 200 |
| a) Odesłanie do miejsca pobrania próbek. Jeżeli nie można użyć kodu NUTS (2), należy określić położenie w stopniach długości i szerokości geograficznej. | |||
3.2.2. Procedury pobierania próbek
1. Do badań wirusologicznych pobiera się wymazy z jamy ustno-gardłowej i z kloaki od ptaków niewykazujących klinicznych objawów choroby, żyjących na wolności. Jeżeli z jakiegokolwiek powodu pobranie wymazów z kloaki od żywych ptaków jest niemożliwe, można je zastąpić zebranymi próbkami świeżego kału. Niemniej należy zapewnić spójność pomiarową w przypadku miejsc mieszania się różnych gatunków ptaków.
2. W celu wyodrębnienia wirusa i wykrycia molekularnego (PCR) pobiera się próbki z kloaki i tchawicy lub jamy ustno-gardłowej lub próbki tkanek (z mózgu, serca, płuc, nerek i jelit) dzikich ptaków padłych lub odstrzelonych.
3. Należy zwrócić uwagę na przechowywanie i transport próbek. Wymazy muszą zostać natychmiast schłodzone lodem lub żelowymi wkładami chłodzącymi i dostarczone do laboratorium w jak najkrótszym czasie. Próbki nie powinny być zamrażane, chyba że jest to bezwzględnie konieczne.
Wymazy muszą być umieszczone (zanurzone całkowicie) w specjalnym podłożu do transportu wirusów lub zbuforowanym płynie fizjologicznym (PBS) z antybiotykami. Umieszczenie próbek we wspomnianym podłożu podczas transportu jest nieodzownym i uzupełniającym działaniem i nie zastępuje schłodzenia.
W razie braku takiego podłoża wymazy należy umieścić w pojemnikach i dostarczyć w postaci suchej.
Jeżeli niemożliwe jest zagwarantowanie szybkiego przewiezienia do laboratorium w ciągu 48 godzin (w podłożu transportowym i temperaturze 4°C), próbki należy niezwłocznie zamrozić, a następnie przewieźć w suchym lodzie. Na przechowywanie i transport mogą wpływać różnorodne czynniki, zatem wybrana metoda musi być odpowiednia do zamierzonego celu.
4. Procedury pobierania próbek przeprowadza się zgodnie z Podręcznikiem diagnostycznym dotyczącym grypy ptaków (decyzja Komisji 2006/437/WE), ustanawiającym procedury diagnostyczne służące do stwierdzenia oraz rozpoznania różnicowego grypy ptaków.
3.3. Opis zastosowanych badań laboratoryjnych
1. Badania laboratoryjne przeprowadza się zgodnie z Podręcznikiem diagnostycznym dotyczącym grypy ptaków (decyzja Komisji 2006/437/WE), ustanawiającym procedury diagnostyczne służące do stwierdzenia oraz rozpoznania różnicowego grypy ptaków.
2. Wszystkie próbki pobrane w ramach programu dotyczącego ptaków dzikich są możliwie najszybciej poddane badaniu przy zastosowaniu technik molekularnych, jeżeli są dostępne, zgodnie z Podręcznikiem diagnostycznym. Badania w kierunku grypy ptaków przeprowadza się w krajowym laboratorium referencyjnym ds. grypy ptaków w PIW-PIB w Puławach. Zaleca się wstępne badanie przesiewowe metodą PCR dla genu M z szybkim przeprowadzeniem badań próbek pozytywnych na identyfikację podtypu H5 i H7 (w terminie 2 tygodni), a w przypadku pozytywnego wyniku jak najszybciej należy przeprowadzić analizę miejsca cięcia hemaglutyniny w celu ustalenia, czy mamy do czynienia z wirusem wysoce zjadliwej grypy ptaków czy nisko zjadliwej grypy ptaków. Jeżeli zostanie potwierdzona obecność wysoce zjadliwej grypy ptaków podtyp H5, należy przeprowadzić dodatkowe badania na określenie podtypu N (nawet jeżeli tym sposobem możliwe jest tylko wykluczenie N1).
3. W laboratorium można pulować do pięciu próbek pobranych od tego samego gatunku ptaków, w tym samym miejscu i czasie, jeżeli zapewniona jest możliwość powtórnego zidentyfikowania i zbadania pojedynczych próbek w przypadku uzyskania pozytywnego wyniku.
4. Opis sytuacji epidemiologicznej w zakresie wysoce zjadliwej grypy ptaków u drobiu w ostatnich pięciu latach
4.1. Środki objęte programem dotyczącym drobiu
W 2007 r. na terytorium Rzeczypospolitej Polskiej wykryto 9 ognisk wysoce zjadliwej grypy ptaków podtypu H5N1 u drobiu hodowlanego. W latach wcześniejszych choroba nie występowała u drobiu hodowlanego. Program nadzoru prowadzony w latach 2003–2010 obejmował fermy kur niosek reprodukcyjnych, kur niosek towarowych, indyków, gęsi i kaczek, strusi, ptaków łownych oraz ptaki dzikie. Próbki były pobierane i badane w ciągu całego roku objętego programem.
4.1.1. Wyznaczenie organu centralnego odpowiedzialnego za realizację programu
Organem centralnym odpowiedzialnym za realizację programu jest Główny Lekarz Weterynarii. Na szczeblu województw organami odpowiedzialnymi za nadzór nad wdrażaniem programu są wojewódzcy lekarze weterynarii. Za właściwe pobieranie i przesyłanie próbek odpowiedzialni są powiatowi lekarze weterynarii.
4.1.2. Wprowadzenie systemu rejestracji gospodarstw
Zgodnie z art. 11 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (Dz. U. z 2008 r. Nr 213, poz. 1342, z późn. zm.) powiatowy lekarz weterynarii prowadzi rejestr podmiotów prowadzących działalność podlegającą nadzorowi.
Rejestr ten zawiera w szczególności:
1) imię, nazwisko, miejsce zamieszkania i adres albo nazwę, siedzibę i adres podmiotu;
2) weterynaryjny numer identyfikacyjny, jeżeli został nadany;
3) określenie rodzaju i zakresu prowadzonej działalności nadzorowanej;
4) informacje o decyzjach administracyjnych wydanych w stosunku do podmiotu;
5) datę wpisu i wykreślenia z rejestru.
Powiatowy lekarz weterynarii przekazuje, za pośrednictwem wojewódzkiego lekarza weterynarii, Głównemu Lekarzowi Weterynarii dane zawarte w rejestrze, a także informacje o każdej zmianie stanu faktycznego lub prawnego ujawnionego w tym rejestrze.
Ponadto powiatowy lekarz weterynarii rejestruje podmioty prowadzące produkcję podstawową. Obowiązek ten wynika z rozporządzenia (WE) nr 853/2004 Parlamentu Europejskiego i Rady z dnia 29 kwietnia 2004 r. ustanawiającego szczególne przepisy dotyczące higieny w odniesieniu do żywności pochodzenia zwierzęcego (Dz. Urz. UE L 139 z 30.04.2004, str. 55, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 45, str. 14) oraz z ustawy z dnia 16 grudnia 2005 r. o produktach pochodzenia zwierzęcego (Dz. U. z 2006 r. Nr 17, poz. 127, z późn. zm.).
4.1.3. Regulacje prawne w zakresie przeprowadzania szczepień
Zgodnie z ustawą z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt grypa ptaków należy do chorób zakaźnych zwierząt podlegających zakazowi szczepień.
5. Sytuacja epidemiologiczna w zakresie choroby u dzikiego ptactwa w ostatnich pięciu latach
5.1. Środki objęte programem dotyczącym dzikiego ptactwa
W 2006 r. wykryto 9 ognisk wysoce zjadliwej grypy ptaków u ptaków dzikich podtyp H5N1. W 2007 r. wykryto jedno ognisko choroby. W latach wcześniejszych wysoce zjadliwa grypa ptaków nie występowała na terytorium Rzeczypospolitej Polskiej. Program dotyczący dzikiego ptactwa w kierunku grypy ptaków w latach 2003–2010 obejmował monitoring czynny oraz bierny.
5.1.1. Wyznaczenie organu centralnego odpowiedzialnego za realizację programu
Organem centralnym odpowiedzialnym za realizację programu jest Główny Lekarz Weterynarii. Na poziomie województw organami odpowiedzialnymi za nadzór nad wdrażaniem programu są wojewódzcy lekarze weterynarii. Za właściwe pobieranie i przesyłanie próbek są odpowiedzialni powiatowi lekarze weterynarii.
5.1.2. Opis i określenie obszarów geograficznych i administracyjnych, na których program zostanie wdrożony
Program dotyczący dzikiego ptactwa realizowany jest na terytorium Rzeczypospolitej Polskiej, z uwagi na fakt, że na całym terytorium państwa występuje duże zagęszczenie gospodarstw hodujących drób. Przeprowadzona analiza potwierdziła, że ryzyko wystąpienia grypy ptaków jest wysokie na obszarze całego państwa. Nadzór u ptaków dzikich podzielony jest na czynny oraz bierny.
6. Regulacje prawne w zakresie powiadamiania o grypie ptaków
Zgodnie z art. 42 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt w przypadku podejrzenia wystąpienia grypy ptaków posiadacz zwierzęcia obowiązany jest do:
1) niezwłocznego zawiadomienia o tym organu Inspekcji Weterynaryjnej albo najbliższego podmiotu świadczącego usługi z zakresu medycyny weterynaryjnej, albo wójta (burmistrza, prezydenta miasta);
2) pozostawienia zwierząt w miejscu ich przebywania i niewprowadzania tam innych zwierząt;
3) uniemożliwienie osobom postronnym dostępu do pomieszczeń lub miejsc, w których znajdują się zwierzęta podejrzane o zakażenie lub chorobę lub zwłoki zwierzęce;
4) wstrzymania się od wywożenia, wynoszenia i zbywania produktów, w szczególności mięsa, zwłok zwierzęcych, środków żywienia zwierząt, wody, ściółki, nawozów naturalnych;
5) udostępnienia organom Inspekcji Weterynaryjnej zwierząt i zwłok zwierzęcych do badań i zabiegów weterynaryjnych, a także udzielania pomocy przy ich wykonywaniu;
6) udzielania organom Inspekcji Weterynaryjnej oraz osobom działającym w imieniu tych organów wyjaśnień i podawania informacji, które mogą mieć znaczenie dla wykrycia grypy ptaków i źródeł zakażenia lub zapobiegania jej szerzeniu.
Wójt (burmistrz, prezydent miasta) niezwłocznie informuje organ Inspekcji Weterynaryjnej o otrzymaniu zawiadomienia.
Zgodnie z art. 51 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt podmioty świadczące usługi z zakresu medycyny weterynaryjnej oraz laboratoria przekazują powiatowemu lekarzowi weterynarii informacje o podejrzeniu wystąpienia grypy ptaków niezwłocznie po powzięciu takiego podejrzenia.
Powiatowy lekarz weterynarii po otrzymaniu zawiadomienia o podejrzeniu wystąpienia grypy ptaków podejmuje natychmiast czynności w celu wykrycia lub wykluczenia grypy ptaków.
Powiatowy lekarz weterynarii natychmiast informuje wojewódzkiego lekarza weterynarii, w tym w formie elektronicznej, o podejrzeniu lub wystąpieniu grypy ptaków oraz o czynnościach podjętych w celu wykrycia lub wykluczenia tej choroby.
Wojewódzki lekarz weterynarii przekazuje natychmiast Głównemu Lekarzowi Weterynarii, w tym w formie elektronicznej, informacje o podejrzeniu lub wystąpieniu grypy ptaków oraz o czynnościach podjętych w celu wykrycia lub wykluczenia tej choroby.
Główny Lekarz Weterynarii:
1) informuje, wykonując postanowienia umów międzynarodowych, których Rzeczpospolita Polska jest stroną, właściwe organizacje międzynarodowe o występowaniu na terytorium Rzeczypospolitej Polskiej grypy ptaków;
2) powiadamia Komisję Europejską oraz inne państwa członkowskie Unii Europejskiej o przypadku wystąpienia grypy ptaków oraz o wygaszaniu ognisk tej choroby.
7. Koszty
7.1. Program dotyczący drobiu
Tabela 10
Środki kwalifikujące się do współfinansowania programu dotyczącego drobiu
| Metody badania laboratoryjnego | Liczba badań do wykonania według danej metody | Koszt jednostkowy badań według danej metody | Koszt jednostkowy badań według danej metody | Koszt całkowity | Koszt całkowity | Finansowanie unijne |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Wstępne serologiczne badanie przesiewowea) | – | – | – | – | – | – |
| Test zahamowania hemaglutynacji HI na obecność H5/H7b) | 19 170 + 960 | 34/1 test | 8,57/1 test | 684 420 | 172 441,42 | tak |
| Test izolacji wirusa (bad. retrospektywne) | 8 | 280 | 70,55 | 2 240 | 564,37 | tak |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Test PCR (bad. retrospektywne) | 16 | 240 | 60,47 | 3 840 | 967,5 | tak |
| Inne środki, jakie mają być objęte | – | – | – | – | – | – |
| Kontrola wyrywkowa | – | – | – | – | – | – |
| Pozostałe | Pobieranie i przesyłanie próbek do laboratorium | 8/próbkę x 9 585 próbek | 2,02/próbkę x 9 585 próbek | 76 680 | 19 319,73 | tak |
| Razem | 767 180 | 193 293,02 | – | |||
| a) Określić badanie laboratoryjne, które należy zastosować. b) Określić liczbę testów na obecność H5 i H7. * Wyliczenie kosztów – według średniego kursu NBP na dzień 3 lutego 2010 r. (1 euro = 3,969 zł). | ||||||
Są to szacunkowe koszty, które zostaną dostosowane do wielkości wydatków przewidzianych na zwalczanie chorób zakaźnych zwierząt w ustawie budżetowej na rok 2011.
7.2. Program dotyczący dzikiego ptactwa
Tabela 11
Środki kwalifikujące się do współfinansowania programu dotyczącego dzikiego ptactwa
| Metody badania laboratoryjnego | Liczba testów do wykonania według danej metody | Koszt jednostkowy testów według danej metody | Koszt jednostkowy testów według danej metody | Koszt całkowity | Koszt całkowity (w euro*) | Finansowanie unijne |
| Wstępne serologiczne badanie przesiewowe | – | – | – | – | – | – |
| Test zahamowania hemaglutynacji HI na obecność H5/H7 | – | – | – | – | – | – |
| Test izolacji wirusa | 20 | 280 | 70,55 | 5 600 | 1 410,93 | tak |
| Badanie PCR | 500 (2000 próbek) | 240 | 60,47 | 120 000 | 30 234,32 | tak |
|
| 50 | 80 | 20,16 | 4 000 | 1 007,81 | |
| Inne środki, jakie należy uwzględnić | – | – | – | – | – | – |
| Kontrola wyrywkowa | – | – | – | – | – | – |
| Pozostałe | Pobieranie i przesyłanie próbek do laboratorium | 20/próbkę x 2000 próbek | 5,04 /próbkę x 2000 próbek | 40 000 | 10 078,11 | tak |
| Razem | 169 600 | 42 731,17 | – | |||
Szacunkowe koszty łącznie (badanie drobiu i ptaków dzikich)*:
767 180 zł + 169 600 zł = 936 780 zł (236 024,19 euro)
Są to szacunkowe koszty, które zostaną dostosowane do wielkości wydatków przewidzianych na zwalczanie chorób zakaźnych zwierząt w ustawie budżetowej na rok 2011.
* Wyliczenie kosztów – według średniego kursu NBP na dzień 3 lutego 2010 r. (1 euro = 3,969 zł).
- Data ogłoszenia: 2011-04-19
- Data wejścia w życie: 2011-04-19
- Data obowiązywania: 2011-08-01
- Dokument traci ważność: 2011-12-31
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA


