REKLAMA
Dziennik Ustaw - rok 2003 nr 134 poz. 1262
ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI1)
z dnia 25 czerwca 2003 r.
w sprawie Centralnej Ewidencji Badań Klinicznych produktów leczniczych weterynaryjnych
Na podstawie art. 6 ust. 5 pkt 1, 3 i 4 ustawy z dnia 6 września 2001 r. – Prawo farmaceutyczne (Dz. U. Nr 126, poz. 1381, z późn. zm.2)) zarządza się, co następuje:
1) wzór zgłoszenia:
a) badań klinicznych produktu leczniczego weterynaryjnego lub przyszłego produktu leczniczego weterynaryjnego,
b) badań pozostałości produktu leczniczego weterynaryjnego w tkankach,
c) innych badań prowadzonych na zwierzętach, których tkanki lub produkty są przeznaczone do spożycia,
do Centralnej Ewidencji Badań Klinicznych produktów leczniczych weterynaryjnych, zwanej dalej „Ewidencją”;
2) sposób i tryb prowadzenia Ewidencji;
3) wysokość opłat za dokonanie wpisu do Ewidencji.
1) badaniu biorównoważności – należy przez to rozumieć badanie, w którym są porównywane produkty lecznicze weterynaryjne lub przyszłe produkty lecznicze weterynaryjne o tej samej postaci farmaceutycznej, zawierające tę samą substancję czynną i produkowane przez różnych wytwórców, prowadzone w celu wykazania, że oba produkty charakteryzują się tą samą biodostępnością;
2) ustawie – należy przez to rozumieć ustawę z dnia 6 września 2001 r. – Prawo farmaceutyczne;
3) podmiocie uprawnionym – należy przez to rozumieć podmiot, o którym mowa w art. 6 ust. 2 ustawy.
2. Po przyjęciu zgłoszenia badania klinicznego Prezes Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, zwany dalej „Prezesem Urzędu”, występuje do niezależnego recenzenta o wydanie opinii na temat zgodności badania z wymaganiami Dobrej Praktyki Klinicznej, określonymi w odrębnych przepisach.
3. Po otrzymaniu opinii niezależnego recenzenta, o której mowa w ust. 2, Prezes Urzędu występuje do ministra właściwego do spraw zdrowia o wydanie decyzji, o której mowa w art. 6 ust. 3 ustawy.
2. Ewidencja obejmuje następujące dane:
1) datę zgłoszenia badania klinicznego do Ewidencji;
2) tytuł badania klinicznego;
3) datę i numer protokołu badania klinicznego;
4) fazę badania;
5) nazwę, siedzibę, adres i oznaczenie formy prawnej prowadzonej działalności albo imię i nazwisko oraz miejsce zamieszkania i adres sponsora i podmiotu uprawnionego;
6) datę otrzymania opinii recenzenta;
7) przewidywany okres prowadzenia badania klinicznego;
8) datę wydania decyzji, o której mowa w art. 6 ust. 3 ustawy;
9) adnotacje związane z przebiegiem badania klinicznego, w szczególności okresy przerw lub zaprzestania badania.
1) z urzędu, na podstawie decyzji ministra właściwego do spraw zdrowia;
2) na wniosek podmiotu uprawnionego, w terminie 7 dni od dnia złożenia go Prezesowi Urzędu.
2. Zmiany w Ewidencji dokonane na wniosek, o którym mowa w ust. 1 pkt 2, obejmują wyłącznie:
1) zmiany niemające wpływu na przebieg badania klinicznego lub zmiany, w których natychmiastowe działanie jest konieczne, aby wyeliminować ryzyko zagrażające zwierzętom lub osobom uczestniczącym w badaniu klinicznym, lub
2) zmiany dotyczące zagadnień technicznych lub administracyjnych.
2. Jeżeli dane, o których mowa w § 5 ust. 2, nie mogą być ze względu na swój zakres ujęte w Ewidencji, stanowią one załącznik do Ewidencji. Osoba prowadząca Ewidencję sporządza w Ewidencji adnotację dotyczącą załącznika.
3. Poprawek w księdze ewidencyjnej dokonuje się w taki sposób, aby wyrazy były poprawiane w sposób czytelny. Osoba dokonująca poprawek opatruje poprawki własnoręcznym podpisem oraz dokonuje stosownej zmiany w Ewidencji prowadzonej w formie systemu informatycznego.
2. Akta ewidencyjne opatruje się numerem zgodnym z numerem wpisu do Ewidencji i przechowuje się w miejscu specjalnie do tego wydzielonym, z zachowaniem przepisów o ochronie informacji niejawnych oraz o ochronie własności przemysłowej.
3. Księgę ewidencyjną i akta ewidencyjne przechowuje się zgodnie z przepisami dotyczącymi klasyfikacji dokumentów do celów archiwalnych.
Minister Rolnictwa i Rozwoju Wsi: A. Tański
|
|
1) Minister Rolnictwa i Rozwoju Wsi kieruje działem administracji rządowej – rolnictwo, na podstawie § 1 ust. 2 pkt 1 rozporządzenia Prezesa Rady Ministrów z dnia 29 marca 2002 r. w sprawie szczegółowego zakresu działania Ministra Rolnictwa i Rozwoju Wsi (Dz. U. Nr 32, poz. 305).
2) Zmiany wymienionej ustawy zostały ogłoszone w Dz. U. z 2002 r. Nr 113, poz. 984, Nr 141, poz. 1181 i Nr 152, poz. 1265 oraz z 2003 r. Nr 45, poz. 391.
Załączniki do rozporządzenia Ministra Rolnictwa i Rozwoju Wsi
z dnia 25 czerwca 2003 r. (poz. 1262)
Załącznik nr 1




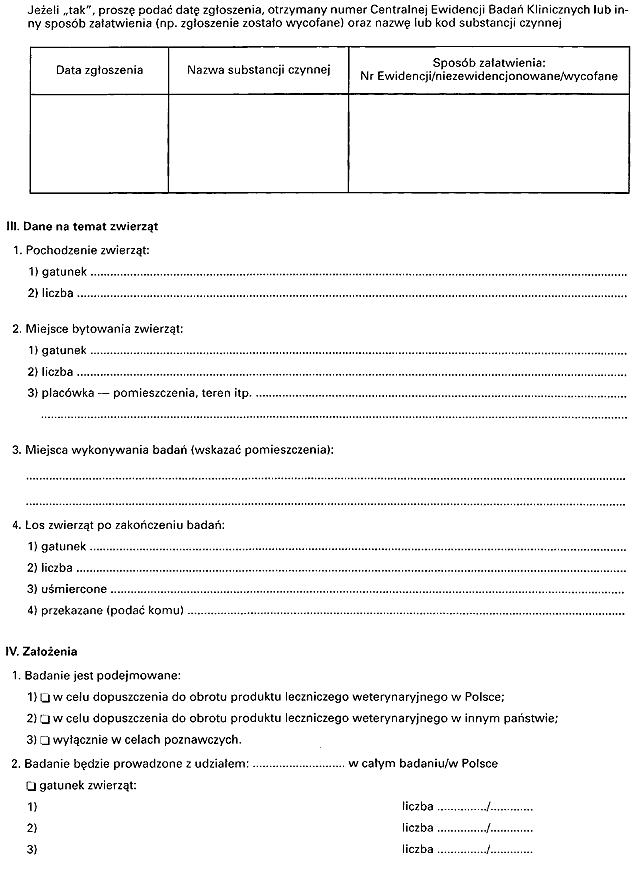



Załącznik nr 2
WYSOKOŚĆ OPŁAT ZA DOKONANIE WPISU DO CENTRALNEJ EWIDENCJI BADAŃ KLINICZNYCH
| Lp. | Wyszczególnienie | Wysokość opłat w zł |
| 1 | Wpis do Ewidencji badania klinicznego oryginalnego produktu leczniczego weterynaryjnego lub przyszłego produktu leczniczego weterynaryjnego | 5000 |
| 2 | Wpis do Ewidencji badania biorównoważności przyszłego produktu leczniczego weterynaryjnego będącego odpowiednikiem referencyjnego produktu leczniczego weterynaryjnego | 2500 |
| 3 | Wpis do Ewidencji badania klinicznego produktu leczniczego weterynaryjnego dopuszczonego do obrotu, przeprowadzonego zgodnie z zatwierdzoną Charakterystyką Produktu Leczniczego Weterynaryjnego | 2500 |
| 4 | Zmiana w dokumentach, wymagająca ponownej oceny wniosku | 500 |
- Data ogłoszenia: 2003-07-31
- Data wejścia w życie: 2003-08-15
- Data obowiązywania: 2003-08-15
- Dokument traci ważność: 2005-03-09
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA
