REKLAMA
Dziennik Ustaw - rok 2003 nr 61 poz. 543
ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI1)
z dnia 26 marca 2003 r.
w sprawie szczegółowych warunków weterynaryjnych wymaganych przy wytwarzaniu pasz leczniczych
Na podstawie art. 5 ust. 4 ustawy z dnia 24 kwietnia 1997 r. o zwalczaniu chorób zakaźnych zwierząt, badaniu zwierząt rzeźnych i mięsa oraz o Inspekcji Weterynaryjnej (Dz. U. z 1999 r. Nr 66, poz. 752, z późn. zm.2)) zarządza się, co następuje:
2. Zlecenie wystawia lekarz weterynarii w trzech egzemplarzach.
3. Oryginał zlecenia przechowuje podmiot, który wytworzył paszę leczniczą, zwany dalej „wytwórcą paszy leczniczej".
4. Dwie kopie zlecenia przechowuje lekarz weterynarii, który wystawił zlecenie.
5. Lekarz weterynarii, który wystawił zlecenie, przekazuje wytwórcy paszy leczniczej oryginał zlecenia i jego kopię. Po wytworzeniu paszy leczniczej wytwórca paszy leczniczej odsyła lekarzowi weterynarii kopię zlecenia.
6. Oryginał zlecenia i jego kopie przechowuje się przez 3 lata od dnia ich wystawienia.
2. Zlecenie jest ważne przez 3 miesiące od dnia wystawienia.
2. Przed wystawieniem zlecenia lekarz weterynarii upewnia się, czy:
1) pasze lecznicze i pasze aktualnie stosowane w żywieniu leczonych zwierząt nie zawierają tego samego antybiotyku lub tego samego kokcydiostatyku jako substancji czynnych;
2) zastosowanie określonej w zleceniu paszy leczniczej jest uzasadnione w odniesieniu do wskazanych w zleceniu gatunków zwierząt;
3) podawanie produktu leczniczego zawartego w paszy leczniczej nie jest sprzeczne z wcześniej zastosowanym leczeniem.
2. Badania, o których mowa w ust. 1, mają na celu ustalenie stopnia wymieszania składników i trwałości paszy leczniczej, a także ustalenie czasu przechowywania paszy leczniczej.
3. Po wykonaniu badań, o których mowa w ust. 1, wytwórca paszy leczniczej prowadzi dokumentację zawierającą informację o:
1) zastosowanej do tych badań metodzie badań laboratoryjnych;
2) wynikach tych badań.
4. Dokumentację, o której mowa w ust. 3, przechowuje się przez 2 lata od dnia wykonania badań.
2. Sposób pobierania i przechowywania próbek archiwalnych, o których mowa w ust. 1, określają przepisy odrębne.
2. Premiks leczniczy, o którym mowa w ust. 1, stosuje się w procesie wytwarzania pasz leczniczych zgodnie z warunkami zezwolenia na dopuszczenie do obrotu.
1) w trakcie wytwarzania paszy leczniczej nie zachodzą niepożądane interakcje między weterynaryjnymi produktami leczniczymi, dodatkami paszowymi i paszami;
2) pasze lecznicze są przechowywane w terminie określonym w zleceniu;
3) pasze wykorzystane do wytwarzania pasz leczniczych nie zawierają tego samego antybiotyku lub kokcydiostatyku, który jest używany jako substancja czynna w premiksach leczniczych.
2. W przypadku przeżuwaczy wytworzona pasza lecznicza zawiera dawkę substancji czynnej odpowiadającą co najmniej połowie dziennego zapotrzebowania leczonego zwierzęcia na niemineralną paszę uzupełniającą.
Minister Rolnictwa i Rozwoju Wsi: A. Tański
|
|
1) Minister Rolnictwa i Rozwoju Wsi kieruje działem administracji rządowej – rolnictwo, na podstawie § 1 ust. 2 pkt 1 rozporządzenia Prezesa Rady Ministrów z dnia 29 marca 2002 r. w sprawie szczegółowego zakresu działania Ministra Rolnictwa i Rozwoju Wsi (Dz. U. Nr 32, poz. 305).
2) Zmiany tekstu jednolitego wymienionej ustawy zostały ogłoszone w Dz. U. z 2001 r. Nr 29, poz. 320, Nr 123, poz. 1350 i Nr 129, poz. 1438, z 2002 r. Nr 112, poz. 976 oraz z 2003 r. Nr 52, poz. 450.
Załącznik do rozporządzenia Ministra Rolnictwa i Rozwoju Wsi
z dnia 26 marca 2003 r. (poz. 543)
WZÓR ZLECENIA NA WYTWORZENIE PASZY LECZNICZEJ

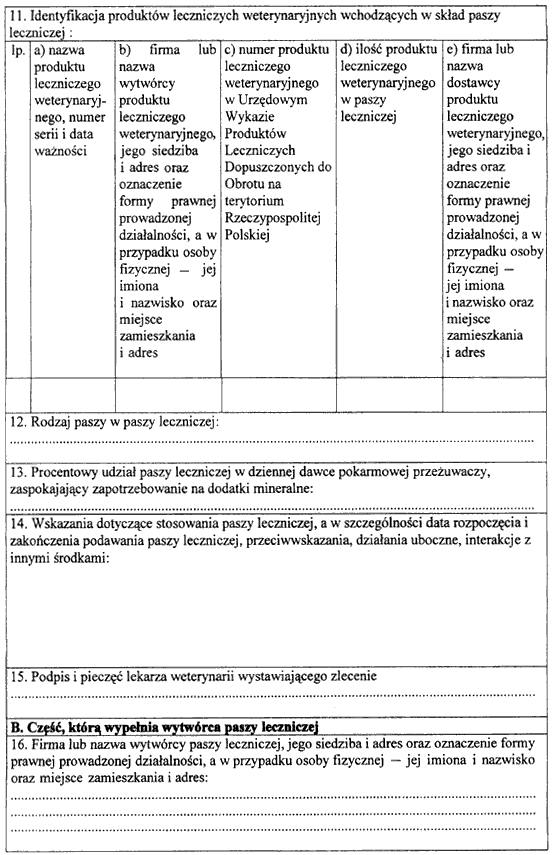

- Data ogłoszenia: 2003-04-10
- Data wejścia w życie: 2003-04-25
- Data obowiązywania: 2003-04-25
- Dokument traci ważność: 2004-04-23
REKLAMA
