REKLAMA
Dziennik Ustaw - rok 2002 nr 234 poz. 1977
ROZPORZĄDZENIE MINISTRA ZDROWIA1)
z dnia 18 grudnia 2002 r.
w sprawie wzorów zgłoszeń rejestrowych do Rejestru Wytwórców i Wyrobów Medycznych oraz wysokości opłat rejestrowych.
Na podstawie art. 30 ust. 2 ustawy z dnia 27 lipca 2001 r. o wyrobach medycznych (Dz. U. Nr 126, poz. 1380 oraz z 2002 r. Nr 152, poz. 1264) zarządza się, co następuje:
2. W zgłoszeniu wyrobu medycznego, o którym mowa w ust. 1, w którego skład wchodzą wyroby medyczne, oznaczone znakiem zgodności CE, wytwórca albo autoryzowany przedstawiciel podaje informację o podstawie oznakowania znakiem zgodności CE.
1) wpisanie numeru nadanego w rejestrze;
2) terminu ważności rejestracji, jeżeli ma to zastosowanie.
2. Zgłoszenia, o których mowa w § 1–5, są kompletne, jeżeli wpisano w nich numer nadany w rejestrze, podano datę dokonania czynności wpisu do rejestru oraz dokonano potwierdzenia poprzez przystawienie pieczęci Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych oraz złożenie podpisu osoby upoważnionej.
2. Ustala się opłaty rejestrowe wnoszone przez wytwórcę albo autoryzowanego przedstawiciela dokonującego zgłoszenia wyrobu medycznego do rejestru:
1) dla wyrobu medycznego oznaczonego znakiem zgodności CE, dla którego wystawiono deklarację zgodności, sklasyfikowanego:
a) do klasy l oraz wyrobu medycznego do diagnostyki in vitro w wysokości 350 zł,
b) do klasy IIa, llb, III oraz aktywnego implantu w wysokości 170 zł;
2) dla wyrobu medycznego, o którym mowa w § 3, w wysokości 350 zł;
3) dla wyrobu medycznego, o którym mowa w § 4 lub § 5, w wysokości 170 zł.
3. Opłatę rejestrową wnoszoną przez wytwórcę albo autoryzowanego przedstawiciela dokonującego zgłoszenia, o którym mowa w § 7, ustala się w wysokości opłaty rejestrowej określone] dla odpowiedniego zgłoszenia, o której mowa w ust. 1 i 2.
Minister Zdrowia: M. Łapiński
|
|
1) Minister Zdrowia kieruje działem administracji rządowej – zdrowie, na podstawie § 1 ust. 2 rozporządzenia Prezesa Rady Ministrów z dnia 28 czerwca 2002 r. w sprawie szczegółowego zakresu działania Ministra Zdrowia (Dz. U. Nr 93, poz. 833).
Załączniki do rozporządzenia Ministra Zdrowia
z dnia 18 grudnia 2002 r. (poz. 1977)
Załącznik nr 1



Załącznik nr 2

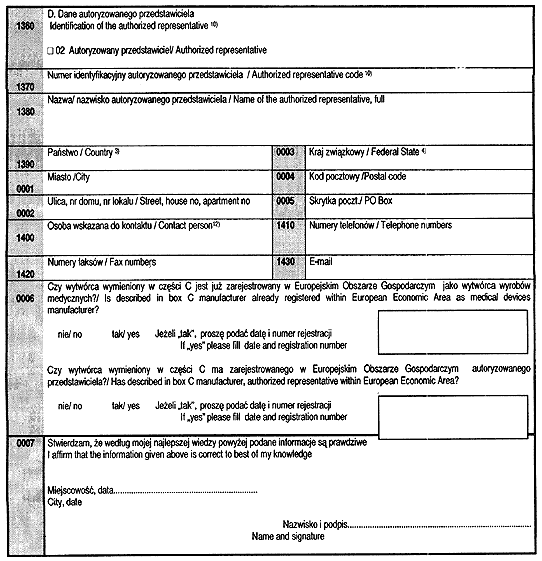
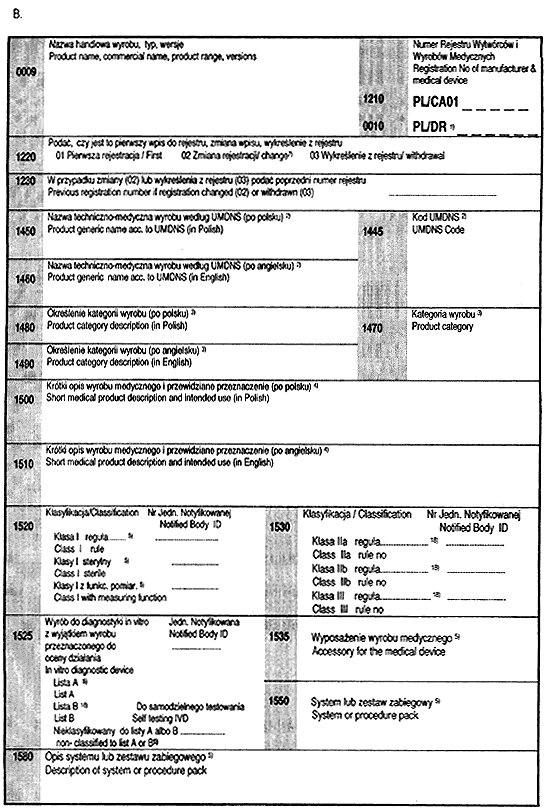


Załącznik nr 3
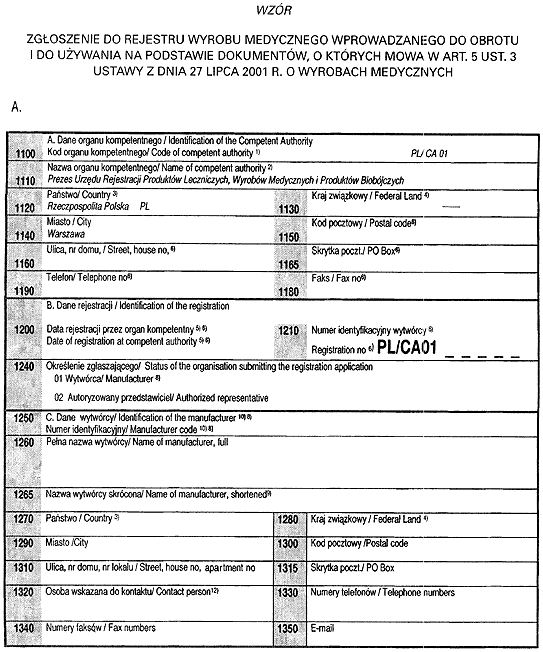



Załącznik nr 4
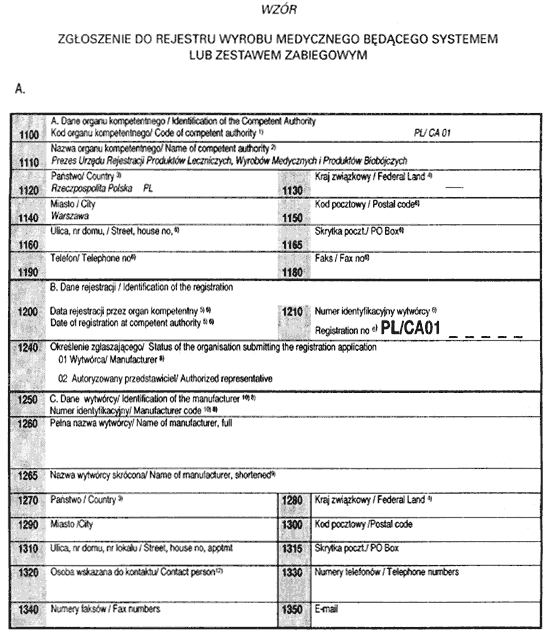



Załącznik nr 5




- Data ogłoszenia: 2002-12-28
- Data wejścia w życie: 2003-01-05
- Data obowiązywania: 2003-01-05
- Dokument traci ważność: 2004-05-01
REKLAMA
